4月5日,國(guó)際學(xué)術(shù)期刊Blood在線發(fā)表了中國(guó)科學(xué)院上海生命科學(xué)研究院(人口健康領(lǐng)域)王蘭研究組的研究論文“Caspase-3 controls AML1-ETO-driven leukemogenesis via autophagy modulation in a ULK1 dependent manner”,該研究發(fā)現(xiàn)Caspase-3能夠通過(guò)切割自噬調(diào)控因子ULK1(ATG1)激酶調(diào)控白血病細(xì)胞自噬從而控制AML1-ETO融合蛋白誘導(dǎo)的t(8;21)急性髓系白血病(AML)的發(fā)生。目前,t(8;21)白血病的治療主要通過(guò)化療或者放療的方式進(jìn)行治療,為了尋找新型有效治療t(8;21)白血病的方法,需要對(duì)其發(fā)生機(jī)制進(jìn)行深入的研究。臨床研究結(jié)果提示出Caspase-3的表達(dá)水平與AML病人的生存期存在著相關(guān)性,低表達(dá)Caspase-3的病人相對(duì)于高表達(dá)Caspase-3的病人具有更長(zhǎng)的生存期。融合蛋白AML1-ETO在t(8:21)白血病干細(xì)胞自我更新的過(guò)程中發(fā)揮著至關(guān)重要的作用,當(dāng)藥物誘導(dǎo)白血病細(xì)胞發(fā)生凋亡時(shí)Caspase-3可以特異性地切割A(yù)ML1-ETO,進(jìn)而增強(qiáng)白血病細(xì)胞對(duì)凋亡信號(hào)敏感性。然而,Caspase-3蛋白本身在白血病發(fā)生的過(guò)程中的作用,在此之前還不是很清楚。因此研究Caspase-3在白血病發(fā)生過(guò)程中的作用及其可能的分子機(jī)制,可以加深我們對(duì)白血病發(fā)生過(guò)程的理解,從而更好地指導(dǎo)白血病的臨床診斷與治療。
研究人員利用遺傳小鼠模型,證明Caspase-3缺失可以延緩t(8;21)白血病的發(fā)生。從分子水平研究揭示Caspase-3能夠直接切割自噬調(diào)控因子ULK1D458位點(diǎn), Caspase-3的缺失能夠促進(jìn)ULK1蛋白激酶的上調(diào),從而促進(jìn)白血病細(xì)胞自噬。白血病中蛋白水解酶Caspase-3,一方面通過(guò)水解ULK1蛋白激酶,另一方面也可以通過(guò)mTOR/P70S6K/4EBP1信號(hào)通路,抑制細(xì)胞自噬發(fā)生。王蘭研究組通過(guò)與邁阿密大學(xué)腫瘤研究中心Stephen Nimer教授合作,證明Caspase-3及其調(diào)控的細(xì)胞自噬信號(hào)通路與白血病發(fā)生緊密相關(guān)。
該研究闡明了蛋白水解酶Caspase-3與細(xì)胞自噬調(diào)控關(guān)鍵信號(hào)分子ULK1,mTOR作用并促進(jìn)白血病發(fā)生的機(jī)理,研究結(jié)果為臨床診斷和治療提供了新的靶點(diǎn)。
該項(xiàng)研究得到了來(lái)自國(guó)家自然科學(xué)基金委、中科院、醫(yī)學(xué)基因組學(xué)國(guó)家重點(diǎn)實(shí)驗(yàn)室以及科技部等科研項(xiàng)目的資助,同時(shí)也得到了上海生科院(人口健康領(lǐng)域)公共技術(shù)平臺(tái)以及動(dòng)物平臺(tái)的支持。(科技處)
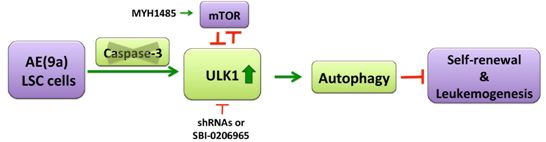
圖示 Caspase-3基因敲除對(duì)通過(guò)影響細(xì)胞自噬控制白血病發(fā)生