2017年4月13日,國際學術期刊Journal of Molecular Cell Biology在線發表了楊黃恬研究組題為“IP3R-mediated Ca2+ signals govern hematopoietic and cardiac divergence of Flk1+ cells via the calcineurin-NFATc3-Etv2 pathway”的最新研究發現。該研究揭示了IP3Rs家族在調控胚胎干細胞(ESCs)向造血和心肌譜系分化命運決定中的重要作用和其作用機制。?
細胞分化命運的決定依賴于多種信號分子和轉錄因子精確而嚴格的調控。鈣離子(Ca2+)是細胞內重要的第二信使,參與調控細胞的增殖、凋亡和分化等多種重要生理過程,但對其在哺乳類細胞的確切調控作用和調控通路了解甚少。ESCs具有自我更新和多能分化的特性,其向特定細胞分化過程重現了體內胚胎早期發育的時空特點和調控模式,因此是解析基因敲除導致胚胎致死基因在發育早期功能的獨特體系,對ESCs分化機制的研究有助于認識胚胎發育的調控機制。三磷酸肌醇受體(IP3Rs)是內質網重要的Ca2+釋放通道。小鼠(m)ESCs中存在三種IP3Rs亞型,亞型間功能既有特異性又存在代償。此前楊黃恬研究團隊發現IP3R3介導的Ca2+釋放通過調控ESCs心肌前體細胞的凋亡影響ESC向心肌譜系的分化,但IP3Rs家族在ESCs特定譜系決定中的精細調控作用和機制尚未闡明。造血和心肌譜系均來自中胚層來源心臟/造血祖細胞(Flk1+)的分化,然而尚不清Flk1+細胞是受何種信號調控從而選擇造血或心肌譜系分化的。?
王毅潔博士和黃吉均博士等在楊黃恬研究員指導下發現ESCs自我更新和三胚層形成并不依賴于IP3Rs,然而造血中胚層(Flk1+/PDGFRa-)的出現依賴于IP3Rs介導的鈣信號,這一鈣信號的缺失抑制中胚層向造血譜系分化但促進其向心肌譜系的分化。在機制方面,IP3Rs釋放的Ca2+而非細胞外的Ca2+內流通過激活鈣調磷酸酶(calcineurin), 進而使得下游的NFATc3結合到調控造血發生的轉錄因子Etv2啟動子促進其表達,進而誘導造血細胞分化而防止心肌細胞分化。研究發現并揭示了IP3Rs在ESCs向造血和心肌這兩種具有同一胚層祖先的譜系命運決定中的重要作用,進一步證實Ca2+信號對于細胞命運調控的重要性和精確性。?
該研究得到了來自國家自然科學基金委、科技部、中國科學院等項目的資助。參與此項工作合作者包括來自北京大學深圳研究生院歐陽昆富研究員和同濟大學高紹榮教授團隊;美國加州大學圣地亞哥分校的陳炬教授提供了Itpr1fl/fl2fl/fl3fl/fl小鼠。
原文鏈接:https://doi.org/10.1093/jmcb/mjx014
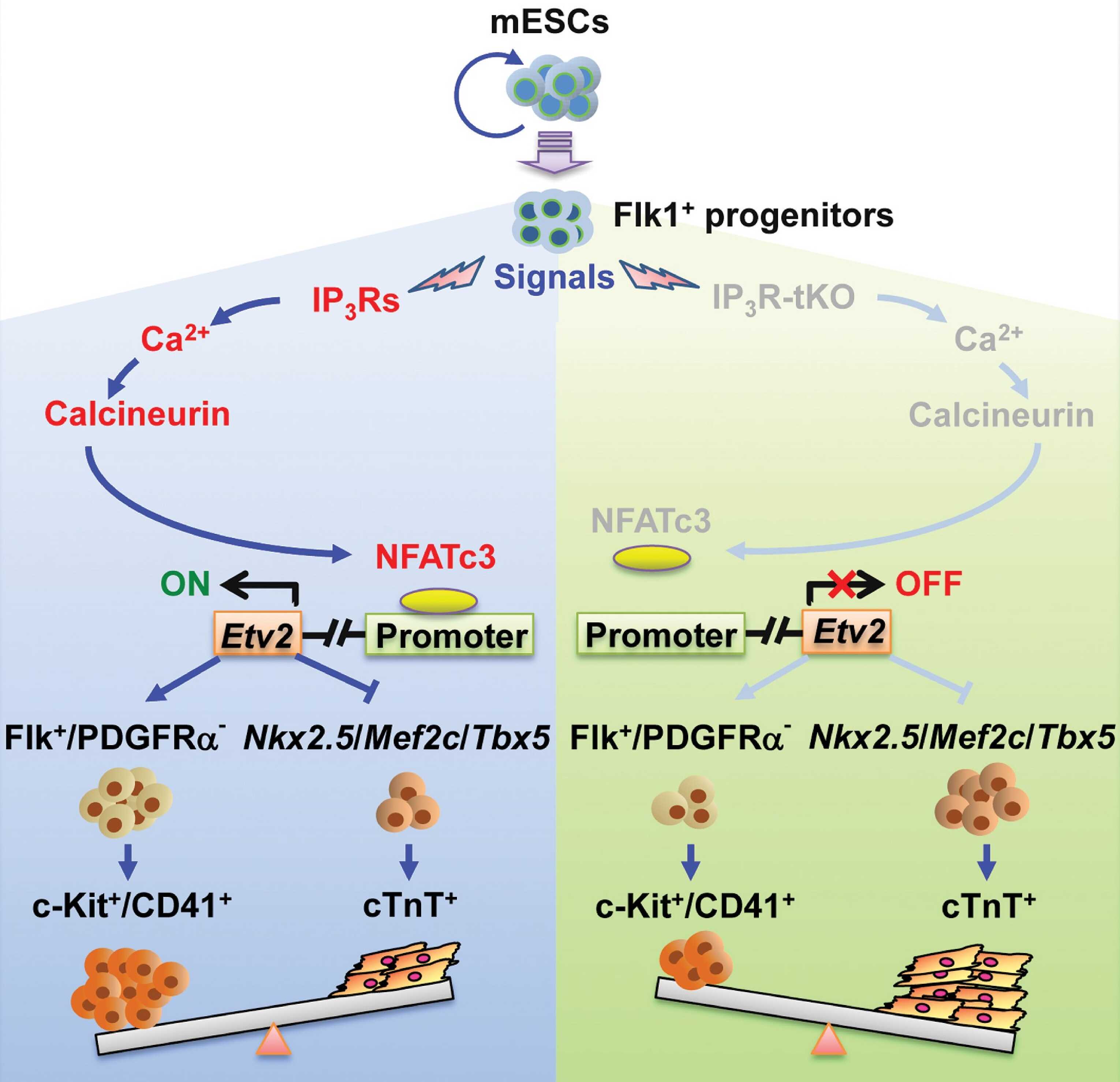
圖. IP3Rs釋放的Ca2+通過calcineurin-NFATc3-Etv2信號通路,調控造血譜系和心肌譜系分化命運決定?