2019年4月18日,中國科學(xué)院上海營養(yǎng)與健康研究所楊力研究員與上海科技大學(xué)生命技術(shù)學(xué)院陳佳教授、上海科技大學(xué)免疫化學(xué)研究所楊貝副研究員,應(yīng)邀在國際知名學(xué)術(shù)期刊《自然-生物技術(shù)》(Nat Biotechnol)上發(fā)表題為“To BE or not to BE, that is the question”的新聞與視角(News and Views)評(píng)論文章,對(duì)近期發(fā)表在Science和Nat Biotechnol上有關(guān)堿基編輯研究的最新進(jìn)展進(jìn)行介紹,并展望了堿基編輯領(lǐng)域未來可能的發(fā)展新方向。
近年來,利用CRISPR/Cas9基因編輯系統(tǒng)與核苷脫氨酶整合而發(fā)展出的新型堿基編輯系統(tǒng)(Base Editor, BE),包括可實(shí)現(xiàn)C-to-T編輯的胞嘧啶堿基編輯器(Cytosine Base Editor, CBE)和實(shí)現(xiàn)A-to-G編輯的腺嘌呤堿基編輯器(Adenine Base Editor, ABE),可在單堿基水平實(shí)現(xiàn)精準(zhǔn)高效的基因組定向編輯。這種新型堿基編輯系統(tǒng),理論上不會(huì)對(duì)基因組DNA造成雙鏈斷裂損傷,且可對(duì)上千種引起人類疾病的基因組堿基突變進(jìn)行定點(diǎn)矯正,因此擁有廣泛的臨床應(yīng)用前景。然而,最近發(fā)表在Science雜志上的兩項(xiàng)研究表明,與傳統(tǒng)的Cas9相比,一種早期構(gòu)建的胞嘧啶堿基編輯器BE3可在小鼠胚胎和水稻的基因組中造成比Cas9更多的非特異性突變,且這些非特異突變的產(chǎn)生不依賴于sgRNA的特異性引導(dǎo)(Zuo et al., Science 2019; Jin et al., Science 2019);而相同條件下的腺嘌呤堿基編輯器卻并沒有產(chǎn)生這些脫靶效應(yīng)(Zuo et al., Science 2019; Jin et al., Science 2019; Kim et al., Nat Biotechnol 2019)。雖然上述發(fā)表的研究中沒有詳細(xì)報(bào)道BE3造成非特異性突變的機(jī)制,在該新聞與視角文章中,陳佳等推測BE3中的胞嘧啶脫氨酶可能通過不依賴sgRNA介導(dǎo)的胞嘧啶脫氨反應(yīng)造成意外的脫靶效應(yīng);并相應(yīng)提出一些降低胞嘧啶堿基編輯器非特異性突變的策略,如通過替換或改造堿基編輯器中的胞嘧啶脫氨酶實(shí)現(xiàn)可控的脫氨活性或與底物DNA結(jié)合的能力等。最后,文章也指出基于低活性胞嘧啶脫氨酶所構(gòu)建的胞嘧啶堿基編輯器,可能無法有效介導(dǎo)在組織器官或者體細(xì)胞(如原代血細(xì)胞)中的基因組靶向堿基編輯。因此,如何發(fā)展新策略構(gòu)建低脫靶率的高效堿基編輯系統(tǒng)將成為堿基編輯領(lǐng)域未來發(fā)展的難點(diǎn)和突破點(diǎn)。
楊力研究員長期從事多組學(xué)生物信息分析研究。近期與上海科技大學(xué)陳佳教授團(tuán)隊(duì)、黃行許教授團(tuán)隊(duì)和楊貝副研究員團(tuán)隊(duì)開展合作,闡明了APOBEC在CRISPR/Cas9引起的基因組DNA斷裂修復(fù)過程中產(chǎn)生突變的分子機(jī)制(Lei et al., Nat Struct Mol Biol 2018),并成功創(chuàng)建多種新型堿基編輯系統(tǒng)(Wang et al., Cell Res 2017; Li et al., Nat Biotechnol 2018; Wang et al., Nat Biotechnol 2018)。
文章鏈接:https://www.nature.com/articles/s41587-019-0119-x
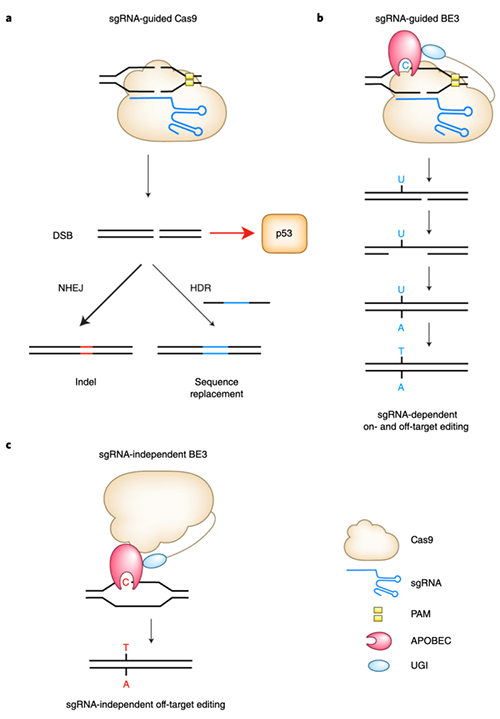
Figure 1 Cas9和堿基編輯器BE3介導(dǎo)的基因編輯比較。
a, Cas9介導(dǎo)的基因編輯與其激活的DNA損傷響應(yīng)。b, BE3在sgRNA依賴性的靶向位點(diǎn)和脫靶位點(diǎn)介導(dǎo)堿基編輯。c, BE3在sgRNA非依賴性的脫靶位點(diǎn)介導(dǎo)堿基編輯。