2019年12月13日,中國(guó)科學(xué)院-馬普計(jì)算生物學(xué)伙伴研究所楊力研究員與上海科技大學(xué)免疫化學(xué)研究所楊貝副研究員和生命科學(xué)與技術(shù)學(xué)院陳佳教授,應(yīng)邀在國(guó)際頂尖學(xué)術(shù)期刊《細(xì)胞》(Cell)上發(fā)表題為《One Prime for All Editing》的專評(píng)論文(Preview),全面地對(duì)哈佛大學(xué)David R.Liu教授近期在Nature 雜志發(fā)表的《Search-and-replace genome editing without double-strand breaks or donor DNA》研究進(jìn)行推介,詳細(xì)解讀了新型基因編輯系統(tǒng)Prime Editing的工作原理,并展望了該領(lǐng)域未來的發(fā)展方向。
在該專評(píng)論文中,楊力研究員等對(duì)Prime Editing系統(tǒng)的設(shè)計(jì)原理及構(gòu)建過程進(jìn)行了介紹(圖1)。新型Prime Editing系統(tǒng)通過將Cas9切刻酶與逆轉(zhuǎn)錄酶融合表達(dá),并利用prime editing guide RNA(pegRNA)最終實(shí)現(xiàn)靶位點(diǎn)的基因編輯。其中,pegRNA由3個(gè)部分組成,包括single-guide RNA(sgRNA)、引物結(jié)合位點(diǎn)(Prime Binding Site,PBS)和儲(chǔ)存有靶向位點(diǎn)編輯信息的反轉(zhuǎn)錄模板(RT templet with edit,圖1A)。Prime Editor(PE)在創(chuàng)建過程中經(jīng)歷了3步關(guān)鍵改進(jìn)。PE1利用Cas9切刻酶(H840A)和Moloney Murine Leukemia Virus(M-MLV)逆轉(zhuǎn)錄酶構(gòu)成,雖可以精確實(shí)現(xiàn)設(shè)計(jì)的基因組編輯,但在哺乳動(dòng)物細(xì)胞上的編輯效率較低。因此,研究人員構(gòu)建了PE2,主要是通過在M-MLV逆轉(zhuǎn)錄酶中引入5個(gè)氨基酸改變進(jìn)而提高靶向位點(diǎn)的編輯效率。最后,研究人員構(gòu)建了PE3/PE3b,通過共表達(dá)介導(dǎo)非靶向DNA單鏈切刻(nick)的sgRNA,利用細(xì)胞內(nèi)源性錯(cuò)配修復(fù)(mismatchrepair)途徑保護(hù)編輯鏈的修飾信息,從而進(jìn)一步提高了primeediting的效率(圖1B)。Primeediting具有非常廣泛的應(yīng)用前景,可以實(shí)現(xiàn)包括12種堿基替換、小片段堿基插入和缺失等的不同編輯用途(圖1C),毋庸置疑地將在基礎(chǔ)和臨床研究領(lǐng)域獲得廣泛地應(yīng)用。在這一專評(píng)論文中,楊力研究員等也指出了Prime Editing系統(tǒng)及其應(yīng)用仍有亟待改進(jìn)之處:如gRNA依賴性或非依賴性的脫靶效應(yīng)尚且未知;PE3介導(dǎo)的高堿基插入/缺失率以及Prime Editing系統(tǒng)在成體動(dòng)物中的遞送等問題。
楊力研究員長(zhǎng)期從事核酸系統(tǒng)生物學(xué)及相關(guān)新技術(shù)拓展研究,近期通過大數(shù)據(jù)整合分析揭示了DNA/RNA堿基編輯及相關(guān)分子機(jī)制(Nat Struct Mol Biol 2018; Mol Cell 2018),利用核酸編輯酶創(chuàng)建多種高效基因組堿基編輯新體系(Cell Res 2017; Nat Biotechnol 2018a; Nat Biotechnol 2018b),并構(gòu)建了可利用20種已報(bào)道堿基編輯器進(jìn)行編輯的人類疾病相關(guān)單堿基突變位點(diǎn)的數(shù)據(jù)庫(kù)(BEable-GPS, Genome Biol 2019)。
楊力研究員、楊貝副研究員和陳佳教授為該論文的共同通訊作者。(科技處)
論文鏈接:https://www.cell.com/cell/fulltext/S0092-8674(19)31287-5
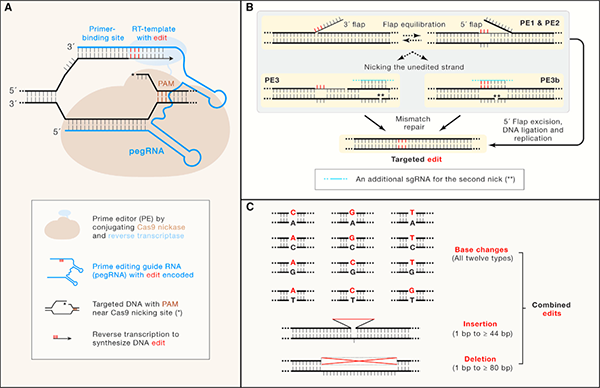
圖1:PE系統(tǒng)的創(chuàng)建與應(yīng)用
(A)PE系統(tǒng)示意圖(B)PE系統(tǒng)的創(chuàng)建歷程(C)PE系統(tǒng)可以介導(dǎo)的編輯類型