2020年5月4日,國際學術期刊Nature Metabolism在線發表了中國科學院上海營養與健康研究所丁秋蓉研究組的研究論文“MRG15 orchestrates rhythmic epigenomic remodeling and controls hepatic lipid metabolism”。該研究發現MRG15作為一個進化上保守的表觀調控因子在調控肝臟組織染色質開放狀態和脂代謝基因轉錄活性的節律性振蕩中行使重要的分子開關作用。研究提示MRG15復合物在肝臟組織感應外界營養狀態,并在營養豐富環境下進行有效能量儲存的過程中起重要作用。該研究為營養過剩環境下脂質代謝紊亂導致的代謝性疾病提供了新的分子靶標。
地球自轉產生了晝夜交替,在長期的進化過程中,生物體產生了生物鐘節律系統,使得行為和生理進程同步于光線的周期變化,以使能量的儲存和利用達到最優狀態。前期研究發現全基因組范圍內的染色質開放和閉合,RNA聚合酶II的基因組結合和新生轉錄活性呈現明顯的晝夜節律。以肝臟為例,基因表達譜分析發現5-20%的基因在肝臟組織中存在24h的振蕩表達,且其中大多數基因對代謝有重要調控作用,說明染色質重塑層面的晝夜節律調控在外周代謝組織中(如肝臟)對代謝基因的整體轉錄調控,繼而能量的儲存和消耗平衡非常重要。而外周代謝組織如何感應外界營養狀態的節律性變化,并在染色質重塑層面做出及時響應是代謝領域有待回答的基本問題。
MRG15是一個進化上非常保守的表觀調控因子,前期被發現參與調控細胞增殖、DNA修復和個體發育過程。雖然MRG15基因附近的基因組區域在人類遺傳學中被鑒定為心血管疾病易感區域,但尚缺乏針對MRG15在代謝中的功能研究。研究人員在系統檢測MRG15基因組結合位點時發現,在肝臟組織中MRG15結合在多個重要脂代謝基因啟動子和增強子區域,并同時發現一個有趣的現象:MRG15的基因組結合呈現明顯的節律性——在小鼠夜間進食狀態下,MRG15結合的基因組位點超過1萬個;而在白天非進食狀態下,MRG15的基因組結合位點只有57個;而改變進食時間能明顯改變MRG15基因組結合的節律性。進一步的研究發現,MRG15與基因組的節律性結合可促進染色質開放,增強RNA聚合酶II的基因組結合,提高基因轉錄活性;而在MRG15敲除的肝臟組織中,全基因組范圍內Pol II基因組結合的節律性被明顯破壞,多個脂代謝基因表達顯著降低,提示MRG15在節律性染色質重塑和脂代謝基因表達調控中起關鍵作用。
研究人員進一步針對導致MRG15節律性基因組結合上游機制進行了研究,初步發現肝臟核受體LRH-1(又名NR5A2)部分介導了MRG15在脂代謝基因轉錄調控區域的結合。LRH-1與MRG15存在蛋白相互作用,實驗結果顯示LRH-1的蛋白表達量以及LRH-1與MRG15的蛋白相互作用明顯受節律和上游營養信號調控,提示了一種經由LRH-1調控MRG15基因組結合的上游營養感應機制。
當通過CRISPR技術在成體小鼠肝臟組織里敲除MRG15進而抑制這一過程后,小鼠能明顯抵抗高脂飲食導致的肝臟脂肪積累,改善代謝平衡。更有意思的是,FDA批準的藥物阿加曲班(argatroban)被發現可以高親和力結合MRG15,抑制MRG15的功能,從而有效抑制肝臟脂滴積累,提示MRG15是一個成藥性較強的分子靶點。綜上,此項研究揭示了肝臟細胞感應上游營養信號,并在染色質重塑水平作出及時響應的一種傳導機制和其間關鍵銜接因子MRG15。
中國科學院上海營養與健康研究所韋余達、田程和趙永旭為該論文的共同第一作者,丁秋蓉研究員為論文通訊作者。這項工作得到了中國科學院上海營養與健康研究所應浩研究員、上海交通大學附屬第六人民醫院劉峰博士和復旦大學于文強教授的大力幫助。該研究還得到了科技部、國家自然科學基金委及中國科學院等項目的資助,同時也得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
原文鏈接:https://www.nature.com/articles/s42255-020-0203-z
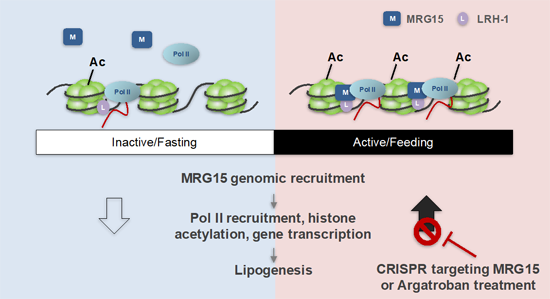
圖1. MRG15是調控肝臟節律性染色質重塑和脂代謝基因表達的表觀分子開關。