2020年12月4日,國際學術期刊PLOS Biology在線發表了中國科學院上海營養與健康研究所尹慧勇研究組題為“Loss of hepatic aldolase B activates Akt and promotes hepatocellular carcinogenesis by destabilizing the Aldob/Akt/PP2A protein complex”的最新研究成果。該研究揭示了糖酵解酶果糖-1,6-二磷酸醛縮酶B(Fructose-1,6-bisphosphate aldolase B, Aldob)通過蛋白相互作用在Akt(Protein kinase B)磷酸化和去磷酸化的平衡中發揮重要的負調節作用。PI3K-Akt信號通路在多種腫瘤中高度激活,其調控機制受到廣泛關注;同時,抑制Akt的活性被認為是一種抗腫瘤的重要策略,多種小分子化合物已經進入臨床試驗。
Aldob是催化糖酵解途徑第四步反應的關鍵酶,催化果糖-1,6-二磷酸(FBP)生成二羥丙酮磷酸(Dihydroxyacetone Phosphate, DHAP)和3-磷酸甘油醛(Glyeraldehyde-3-phosphate, GAP),以及糖異生中由DHAP與GAP生成FBP的逆反應。該研究組前期研究發現Aldob通過結合磷酸戊糖途徑中限速酶葡萄糖-6-磷酸脫氫酶(Glucose-6-phosphate dehydrogenase, G6PD)并抑制其酶活,在調控肝細胞癌(Hepatocellular Carcinoma, HCC)代謝重構中發揮重要作用(Li et al, Nature Cancer, 2020, 1: 735-747)。然而,調控肝癌代謝重構的上游信號通路尚未明確。
在本研究中,研究人員在全身和肝特異敲除ALDOB的小鼠腫瘤組織中觀察到Akt及其下游信號通路的激活。在體外細胞實驗中發現Aldob顯著降低Akt磷酸化及其激酶活性,抑制細胞增殖、葡萄糖攝取與代謝。進一步的機制研究發現,Aldob通過直接結合Akt來抑制其激酶活性。而且,Aldob優先與磷酸化的Akt (p-Akt) 相互作用,招募蛋白磷酸酶2A (Protein phosphatase 2A, PP2A) 去磷酸化p-Akt,從而使Akt維持在失活狀態。本研究表明Aldob與Akt相互作用,通過調節底物Akt與其蛋白激酶和磷酸酶的相互作用,參與調控Akt磷酸化和去磷酸化的平衡。而在HCC細胞中,Aldob的表達下調解除其對Akt活性的負調控,引起致癌Akt信號傳導通路異常活化,從而促進細胞增殖、葡萄糖攝取和代謝(如圖一所示)。與上述機制一致,在臨床HCC病人腫瘤樣本中Aldob和p-Akt的蛋白表達水平呈負相關,并且Aldob低表達、p-Akt高表達與HCC患者預后不良顯著相關。此外,研究人員利用一種新型PP2A小分子激活劑SMAP,在體外和體內實驗中均能有效激活PP2A磷酸酶活性,抑制Akt信號通路及腫瘤細胞生長。綜上,本研究發現了Aldob在肝癌發生過程發揮非代謝酶功能的新機制,同時為激活PP2A磷酸酶活性作為新型靶向治療HCC策略提供了初步證據。有趣的是, 實驗室前期的一項研究發現花生紅衣多酚原花青素B2可以直接結合Akt并抑制其活性,在肝癌模型中發揮抗癌作用(Liu et al, Redox Biology, 2020; 37: 101701)。
中國科學院上海營養與健康研究所尹慧勇研究員、陶用珍助理研究員與海軍軍醫大學第三附屬醫院程樹群主任為該論文通訊作者,中國科學院上海營養與健康研究所博士研究生何栩曉、李敏為該論文共同第一作者。該項工作得到了美國密西根大學Goutham Narla教授的大力支持。此課題研究得到了國家自然科學基金委、科技部和中國科學院的資助。(科技處)
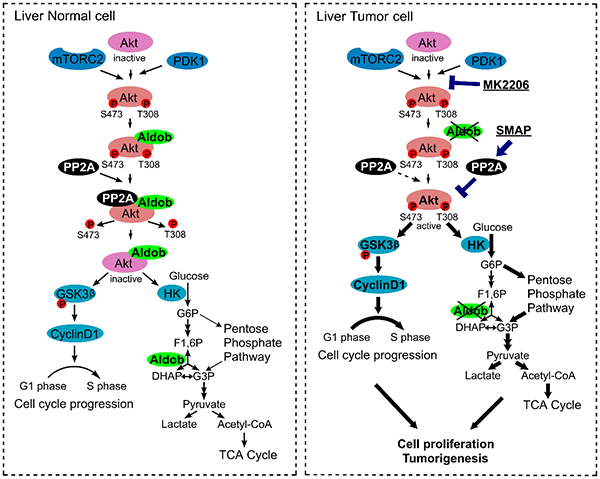
圖一. 醛縮酶B調控肝癌Akt信號通路新機制。在正常肝細胞中, Aldob除了發揮代謝酶功能外還與Akt結合, 招募蛋白磷酸酶PP2A去磷酸化p-Akt, 防止其過度激活。在肝癌腫瘤細胞中,Aldob的丟失造成Akt的激活,促進腫瘤細胞增殖與葡萄糖代謝。利用Akt的別構抑制劑MK2206抑制Akt的酶活,或者PP2A的激活劑SMAP激活的PP2A活性均可以抑制由于Aldob丟失引起的肝癌。
論文鏈接:https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3000803