2022年
10月
6日,中國科學院上海營養與健康研究所孫宇研究團隊在學術期刊
Oncogene正式發表了題為
“Targeting epiregulin in the treatment-damaged tumor microenvironment restrains therapeutic resistance”的研究論文。該研究發現了微環境中一種全新的衰老相關分泌因子在組織微環境中的產生基礎以及其對腫瘤惡性進展的作用機制。
細胞衰老是一種獨特的細胞狀態,具有多種明確且穩定的細胞特征。其中,衰老相關分泌表型 (Senescence-associated secretory phenotype, SASP),使其在微環境中可對其他細胞發揮復雜的信號傳遞功能。在老年人群中,包括慢性炎癥形成過程以及腫瘤微環境的局部空間內,SASP這一分泌表型對多種疾病的進展均造成不可忽視的病理作用。因而,研究SASP相關因子以及其在腫瘤等疾病的組織微環境中發揮功能的分子機制和干預途徑,對老年疾病的臨床治療具有深遠的指導意義。
該研究通過對人類原代基質細胞進行基于結合當前臨床化療脅迫壓力的體外藥物模擬處理,確認了epiregulin (EREG)在DNA損傷類型的衰老誘導條件下顯著表達上調,而過往尚未有報道該因子與微環境中衰老細胞之間存在關聯。同時,對臨床前列腺癌及乳腺癌患者化療前后癌癥樣本的分析,也發現EREG在衰老的癌旁基質細胞中顯著上調表達。機制上,DNA損傷導致基質細胞中轉錄因子NF-κB等發生核轉位并結合在EREG啟動子區多個位點,進而促進EREG在細胞衰老后表達上調。同時,研究人員也注意到其他衰老相關因素包括:轉錄因子C/EBP激活,DNA空間開放度變化及表觀遺傳修飾改變對EREG轉錄起到促進作用。
在腫瘤微環境中,衰老細胞釋放的EREG通過與其附近的癌細胞表面EGFR受體結合激活包括MAPK、AKT/mTOR及JAK/STAT等多條下游信號通路,從而誘發癌細胞增殖、遷移、侵襲等惡性表型,并最終造成癌細胞顯著的耐藥能力。通過RNA-Seq分析,研究人員發現了一種泛素連接酶MARCHF4在基質EREG激活的癌細胞中顯著表達上調。MARCHF4可以使得癌細胞E-cadherin表達下調并抑制癌細胞凋亡,因而導致腫瘤耐藥現象發生。在小鼠模型中,EREG單克隆抗體及EGFR單克隆抗體的聯用顯著降低腫瘤體積并顯著延長了小鼠無病進展生存期。值得一提的是,癌癥患者體內微環境中EREG的表達水平與其臨床治療后階段的長期生存之間存在顯著的負相關,并可作為對患者(包括多種癌型)預后的一個新型的標記物。
綜上,這項工作深入發現并準確闡釋了微環境中的衰老相關分泌因子EREG在腫瘤微環境中的病理功能及其調控機制,并揭示了其在將來轉化醫學和臨床應用中的巨大潛力和重要價值。中科院上海營養與健康研究所博士生王常旭和復旦大學中山醫院泌尿外科龍啟來為該論文共同第一作者。上海營養與健康研究所孫宇研究員為該論文的通訊作者。該項工作得到了國家科學技術部、國家自然科學基金委、中科院戰略性先導科技專項和上海市科委等部門的經費資助,以及營養與健康所所級中心公共技術平臺的支持。
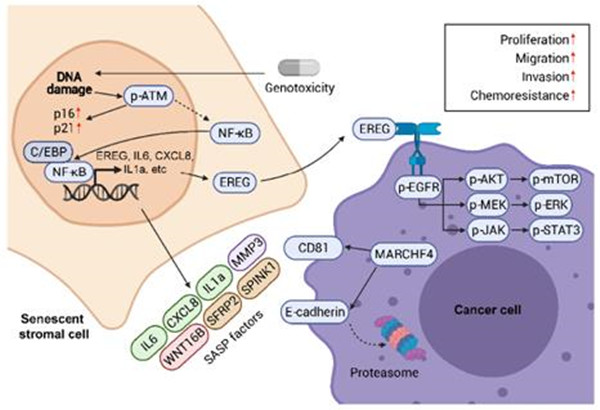
圖注: 當代臨床藥物等治療方式(尤其基因毒化療)誘導損傷的腫瘤微環境中,基質細胞EREG表達上調并通過旁分泌方式激活附近癌細胞,促進其惡性表型并加速疾病進展;EREG將來可以作為患者療后階段的監測指標和臨床抗癌治療的新靶點。
論文鏈接:https://doi.org/10.1038/s41388-022-02476-7