2022年11月9日,國(guó)際學(xué)術(shù)期刊Leukemia在線發(fā)表了中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所王蘭研究組題為“Inhibition of USP1 reverses the chemotherapy resistance through destabilization of MAX in the relapsed/refractory B cell lymphoma”的最新研究成果。我們的研究闡明了去泛素化酶USP1在利妥昔單抗/化療耐藥B細(xì)胞淋巴瘤中的關(guān)鍵作用,為利妥昔單抗/化療耐藥彌漫大B細(xì)胞淋巴瘤(DLBCL)提供了一種新的治療策略。
淋巴瘤是一種起源于淋巴細(xì)胞的惡性腫瘤,分為霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL)。彌漫性大b細(xì)胞淋巴瘤是最常見的淋巴瘤亞型,占NHL的30-35%。近年來,6-8個(gè)周期的R-CHOP方案(利妥昔單抗、環(huán)磷酰胺、阿霉素、長(zhǎng)春新堿和潑尼松)已成為DLBCL的標(biāo)準(zhǔn)治療方案,并取得了良好的療效。然而,一些預(yù)后較差的DLBCL患者在短期緩解后仍然對(duì)治療有耐藥性或復(fù)發(fā)。因此,識(shí)別與DLBCL患者預(yù)后和R-CHOP方案療效相關(guān)的標(biāo)志物非常重要,這最終將有助于探索利妥昔單抗/化療耐藥DLBCL的新靶向治療方法。
在本研究中,研究人員發(fā)現(xiàn)泛素特異性蛋白酶1 (USP1)在復(fù)發(fā)/難治性彌漫性大B細(xì)胞淋巴瘤(DLBCL)患者中高表達(dá),并且USP1高表達(dá)與DLBCL患者不良預(yù)后顯著相關(guān)。在本研究中,USP1缺失顯著抑制了DLBCL細(xì)胞的增殖,誘導(dǎo)細(xì)胞周期阻滯,激活細(xì)胞自噬,在DLBCL小鼠移植瘤模型中,敲低DLBCL細(xì)胞中的USP1顯著抑制裸鼠淋巴瘤的生長(zhǎng)。隨后,在機(jī)制上,研究人員發(fā)現(xiàn)USP1與MAX相互作用,通過去泛素化修飾維持MAX/MYC異二聚體的穩(wěn)定性,從而調(diào)節(jié)MYC靶基因的轉(zhuǎn)錄。
為了研究USP1在DLBCL中的靶向治療效果,研究人員使用USP1特異性抑制劑pimozide進(jìn)行實(shí)驗(yàn),研究發(fā)現(xiàn)pimozide可顯著抑制DLBCL細(xì)胞增殖,誘導(dǎo)細(xì)胞周期阻滯,增加細(xì)胞自噬,pimozide處理還可以顯著阻礙DLBCL細(xì)胞或者患者腫瘤異種移植小鼠模型的腫瘤增殖。此外,pimozide與etoposide等化療藥物在體外和體內(nèi)均具有協(xié)同作用。綜上所述,該研究揭示了USP1在利妥昔單抗/化療耐藥DLBCL中的關(guān)鍵作用,USP1抑制劑pimozide可能對(duì)臨床利妥昔單抗/化療耐藥DLBCL的治療具有重要指導(dǎo)意義。
中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所王蘭研究員和復(fù)旦大學(xué)附屬腫瘤醫(yī)院腫瘤內(nèi)科張群嶺主任醫(yī)師為該論文的共同通訊作者,中科院上海營(yíng)養(yǎng)與健康所博士研究生李西亞、博士畢業(yè)生吳記傳、博士研究生劉平為該論文第一作者。這項(xiàng)工作得到了多家醫(yī)療和科研單位合作者的大力支持包括羅斯威爾帕克癌癥研究所的顧雋教授,上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院的王黎主任醫(yī)師。此課題得到了國(guó)家自然科學(xué)基金委、科技部,上海市“科技創(chuàng)新行動(dòng)計(jì)劃”和中國(guó)科學(xué)院和資助。
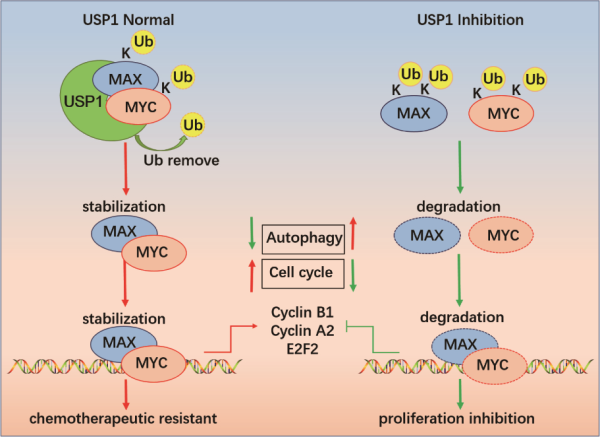
圖. USP1調(diào)節(jié)DLBCL的分子機(jī)制示意圖