2022年12月1日,國際學術期刊Advanced Science在線發表了中國科學院上海營養與健康研究所謝東研究組題為“PPDPF promotes the development of mutant KRAS-driven pancreatic ductal adenocarcinoma by regulating the GEF activity of SOS1”的研究成果。該研究揭示了PPDPF在胰腺導管腺癌發生發展中的重要作用,并為KRAS突變的PDAC患者提供了有潛力的治療策略。
胰腺癌是世界上最惡性的腫瘤之一,胰腺導管腺癌(pancreatic ductal adenocarcinoma,PDAC)約占胰腺癌的95%以上。PDAC患者5年總生存率不到5%。雖然手術是有效延長PDAC患者生存時間的唯一治療手段,但腫瘤手術切除患者的5年生存率仍低于25%。盡管人們對胰腺癌的機制認識有了實質性的提高,但目前胰腺癌的治療方法仍然非常有限。因此,探索胰腺導管腺癌發生發展的分子機制,有助于為PDAC的治療提供潛在的分子靶點。
RAS基因是人類癌癥中最常發生突變的致癌基因。98%的PDAC患者中KRAS發生突變,其中G12位點突變占KRAS突變的97%。SOS1是RAS的一個重要的鳥嘌呤核苷酸交換因子(guanine nucleotide exchange factors, GEF),通過將RAS結合的GDP轉換為GTP,從而激活RAS。EGF激活EGFR后,SOS1被招募到細胞膜上,并催化RAS結合的GDP-GTP交換。CDC25和REM結構域是SOS1的核心結構域(合稱為Cat結構域),發揮催化功能。REM結構域包含一個能夠與RAS-GTP結合的激活異構位點。該位點結合RAS-GTP后,可進一步激活負責催化的CDC25結構域,進而促進RAS的GDP-GTP交換。SOS1的GEF活性受到不同機制的調控,包括SOS1的膜定位、自抑制及MAPK對SOS1的C端結構域的磷酸化等。之前的研究顯示GEF可以結合GTP。然而,目前對于GEF結合GTP的意義,以及SOS1是否能夠結合GTP尚不清楚。
胰腺祖細胞分化與增殖因子(PPDPF)首次在斑馬魚中被報道。PPDPF是一種外分泌細胞決定因子,具有潛在的PDZ, SH2, SH3和GTP結合位點。但是PPDPF在胰腺癌中的生物學功能尚不清楚。
本研究發現PPDPF在胰腺癌中的表達顯著升高,PPDPF高表達的患者預后較差。在胰腺導管腺癌小鼠模型中敲除Ppdpf顯著抑制Kras突變驅動的PDAC的發生發展。此外,研究人員還證明了PPDPF可以結合GTP,并將GTP提供給SOS1,從而增強其GEF活性,促進KRAS的活化。該項研究揭示了PPDPF在PDAC中的新功能和KRAS活化調控的新機制,為PDAC提供了一個潛在的治療靶點。
中國科學院上海營養與健康研究所博士倪謙枝和博士生朱兵為文章的共同第一作者,中國科學院上海營養與健康研究所李晶晶副研究員和謝東研究員為本文的通訊作者。該研究獲得了國家自然科學基金委和中國科學院的經費支持,同時也得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
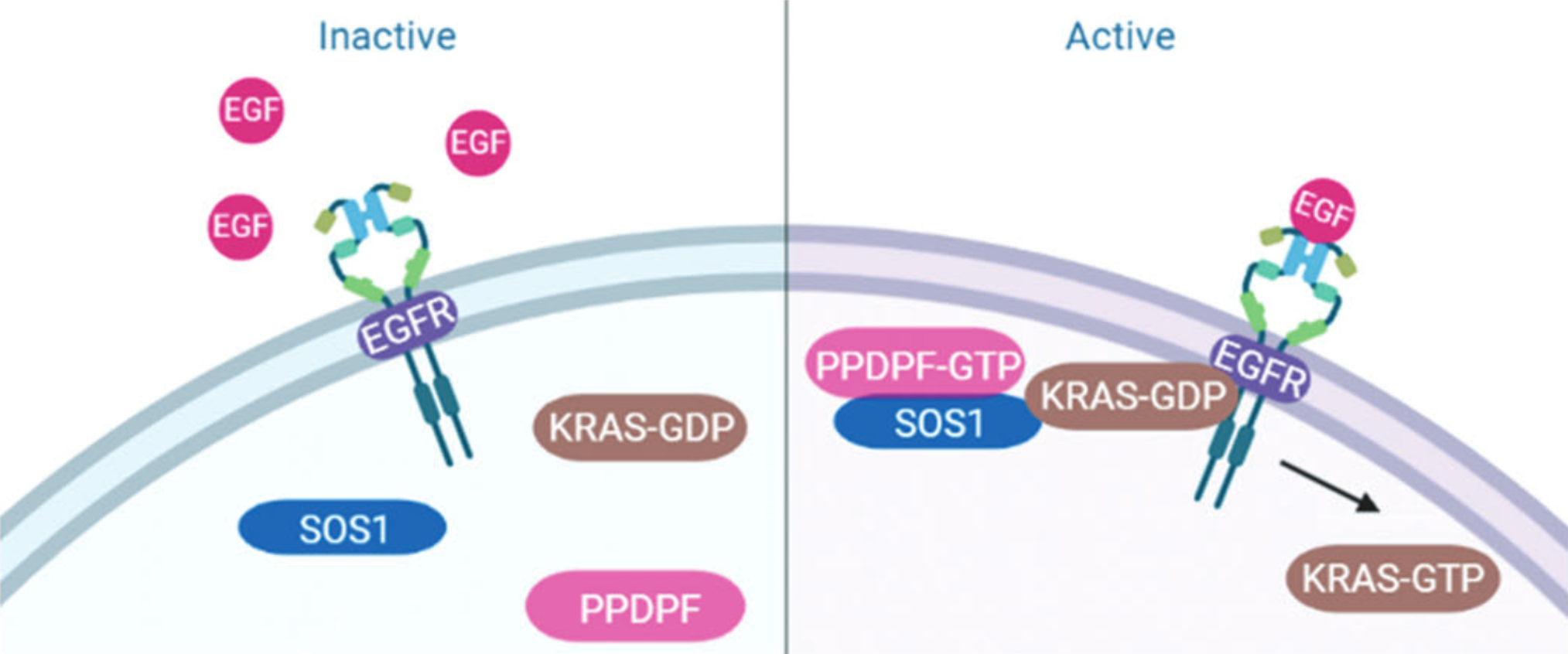
????圖. PPDPF調控KRAS活化的機制示意圖