2023年2月13日,國際學術(shù)期刊Cell Stem Cell在線發(fā)表了我所李虹研究組、李亦學研究組與中國科學院分子細胞科學卓越創(chuàng)新中心惠利健研究組合作的研究文章“Kupffer cell-derived IL-6 is repurposed for hepatocyte dedifferentiation via activating progenitor genes from injury-specific enhancers”。該研究揭示肝臟損傷下,駐留巨噬細胞分泌的炎癥信號IL-6誘導了肝細胞的去分化。IL-6激活STAT3信號通路,STAT3結(jié)合在損傷特異的增強子上誘導了肝前體基因的表達。
肝臟在損傷情況下,組織再生的細胞來源一直是領(lǐng)域內(nèi)的研究焦點。目前認為穩(wěn)態(tài)的肝臟內(nèi)不存在肝干細胞,新生肝細胞主要來源于已分化的上皮細胞。成熟肝細胞能在損傷條件下發(fā)生去分化,重編程為Sox9+類肝前體細胞 (Liver progenitor-like cells, LPLCs)。但LPLC的形成過程、不同細胞狀態(tài)特異表達的基因、細胞狀態(tài)轉(zhuǎn)換相關(guān)的基因及分子機制還有待深入研究。單細胞測序技術(shù)及生物信息分析能夠捕獲組織內(nèi)表達的各種細胞狀態(tài),是研究上述問題的有力工具。
在該工作中,研究人員通過對單細胞轉(zhuǎn)錄組測序數(shù)據(jù)的深入分析,鑒定了健康肝臟和損傷肝臟中不同的肝細胞亞群,并從中鑒定出一組高表達Sox4,Sox9,Spp1,Cd24a等干性相關(guān)基因的肝細胞亞群。該細胞類群與之前報道的Sox9陽性類肝前體細胞 (Liver progenitor-like cells, LPLCs)高度相似,因此認為是LPLCs。通過偽時序分析,研究人員首次重塑了正常肝細胞經(jīng)損傷后重編程(reprogramming)轉(zhuǎn)變?yōu)長PLCs的過程。通過對生物學通路富集打分與細胞偽時間(pseudotime)進行建模,得到重編程過程中顯著變化的信號通路,發(fā)現(xiàn)損傷下免疫信號通路與重編程高度相關(guān)。另外,通過比較Non-LPLCs肝細胞,鑒定出了reprogramming related genes。這些為后續(xù)機制實驗的開展提供了線索和方向。之后,研究人員對肝臟的不同免疫細胞進行了復雜的敲除實驗,發(fā)現(xiàn)肝臟駐留Kupffer細胞(KCs)是LPLCs出現(xiàn)所必要的,而阻斷單核來源的巨噬細胞(MoMFs)及其他免疫細胞對LPLCs出現(xiàn)無影響。通過解析肝損傷下巨噬細胞的單細胞測序數(shù)據(jù)及大塊組織樣本測序數(shù)據(jù),結(jié)合體內(nèi)篩選實驗,研究人員發(fā)現(xiàn)IL-6可以在無損傷的肝臟內(nèi)直接結(jié)合肝細胞IL6R/gp130誘導LPLCs的出現(xiàn),其下游是通過STAT3信號轉(zhuǎn)導實現(xiàn)。之后,利用ChIP-seq技術(shù),研究人員證明STAT3能夠結(jié)合重編程基因預先開放的染色質(zhì)區(qū)域。有趣的是,研究人員發(fā)現(xiàn)胚胎發(fā)育過程中STAT3并未激活,組蛋白H3K27ac修飾在LPLCs相關(guān)的增強子區(qū)域也未激活,說明了肝臟損傷下IL-6/STAT3信號是結(jié)合了損傷特異的增強子誘導了前體基因的表達。本研究揭示了肝臟損傷下巨噬細胞的炎癥信號通過損傷特異的轉(zhuǎn)錄調(diào)控模式誘導肝細胞去分化的機制,該機制為探索誘導體內(nèi)重編程的因子,開發(fā)治療肝臟疾病相關(guān)藥物,奠定了重要的理論基礎(chǔ)。
中國科學院分子細胞科學卓越創(chuàng)新中心博士李露(已畢業(yè)),在讀博士崔磊和中國科學院上海營養(yǎng)與健康研究所博士后林平為該論文共同第一作者,中國科學院分子細胞科學卓越創(chuàng)新中心惠利健研究員,中國科學院上海營養(yǎng)與健康研究所李虹研究員和李亦學研究員為該論文通訊作者。該工作得到中國科學院、基金委、科技部、上海市科委、上海發(fā)改委等經(jīng)費支持。
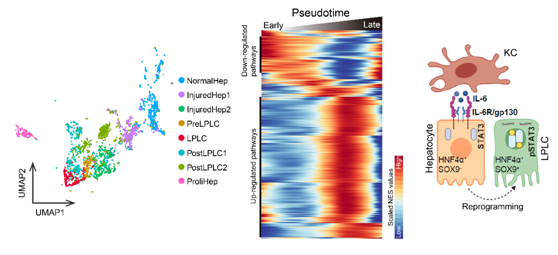
肝臟損傷條件下駐留巨噬細胞分泌的炎癥信號IL-6誘導了肝細胞的去分化
文章鏈接:
https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(23)00009-7