中國科學院上海營養與健康研究所、西南醫科大學附屬醫院和青島大學研究人員首次解析脯氨酸羥基化修飾調控2型糖尿病進展的新機制,揭示了脯氨酸羥化酶3(PHD3)通過羥基化增加糖異生關鍵轉錄因子CRTC2的核定位與活性,進而增加肝臟糖異生基因表達和葡萄糖產生。該研究成果于5月30日在《美國科學院院刊》(PNAS)在線發表。
肝臟作為重要的內分泌器官,肝臟糖代謝在維持機體血糖穩態中扮演著重要角色。肝臟糖異生過度增加是導致高血糖和2型糖尿病的重要原因。胰高血糖素的分泌會通過激活PKA通路和增加CREB的磷酸化來促進CREB與其轉錄輔因子CRTC2的結合,進而促進糖異生關鍵限速酶PEPCK和G6Pase的表達,增加糖異生水平。脯氨酸羥化酶PHD3能夠通過感應氧氣含量的變化來調節缺氧誘導因子HIF的羥基化水平,從而影響其活性。然而,PHD3能否感應機體其它生理狀態變化并調控機體葡萄糖代謝與血糖穩態尚不清楚。
為了探究PHD3是否能夠感應機體能量的變化,研究人員首先檢測了正常飼喂和禁食狀態下小鼠肝臟中PHD3的蛋白水平,發現禁食能顯著增加PHD3的蛋白表達。利用PHD3肝細胞特異性敲除小鼠,分別進行禁食和高脂高蔗糖飲食喂養,發現無論是在禁食的生理狀態還是肥胖的病理狀態下,PHD3肝細胞特異性敲除均能降低小鼠肝臟中糖異生關鍵酶的表達水平和減少葡萄糖生成。其次,為了探究PHD3的作用是否通過其羥化酶活性來發揮,研究人員進一步構建了PHD3肝細胞羥化酶活性缺失的基因敲入(KI)小鼠模型,得到了和PHD3肝細胞特異性敲除小鼠一致的結果,表明PHD3參與糖異生的調控過程依賴其羥化酶活性。進一步的機制研究發現,PHD3通過羥基化CRTC2的Pro129和Pro625位點,促進CRTC2與CREB結合,增加CRTC2的核轉位與轉錄活性,從而增加糖異生基因轉錄和葡萄糖生成。此外,CRTC2 Pro615位點的羥基化水平在禁食小鼠、ob/ob肥胖的糖尿病小鼠、糖尿病病人肝臟組織中均顯著增加,這表明在生理和病理條件下,PHD3介導的CRTC2羥基化修飾可能在小鼠及人的血糖穩態調控中均發揮重要作用。
該研究發現糖異生關鍵轉錄因子CRTC2是PHD3新的下游底物,羥基化修飾增強了CRTC2的核轉位與活性,從而增加糖異生基因的表達和肝糖輸出。同時,該研究表明抑制肝臟PHD3或CRTC2羥基化可能是治療高血糖和2型糖尿病的新策略。蛋白質翻譯后修飾與2型糖尿病等代謝性疾病的發生和發展密切相關。李于研究組之前研究發現,AMPK通過磷酸化修飾脂質合成代謝關鍵因子Insig和SREBP,抑制肝臟脂質過度合成和非酒精性脂肪肝(Nat Commun, 2019; Cell Metab, 2013)。這些研究揭示蛋白翻譯后修飾關鍵酶(如PHD3和AMPK)調節糖脂代謝紊亂的分子機制,為防治2型糖尿病和脂肪肝等代謝性疾病提供新的思路和治療手段。
中國科學院上海營養與健康研究所李于研究員、西南醫科大學附屬醫院付文廣教授、青島大學方靖教授為本論文通訊作者,中國科學院上海營養與健康研究所薛雅倩博士和崔奧媛副研究員為本論文第一作者。該研究得到國家科技部重點研發計劃、國家自然科學基金委、上海市市級重大專項、代謝性血管疾病四川省重點實驗室開放課題、山東省自然科學基金委、中國博士后科學基金的支持,同時得到中國科學院上海營養與健康研究所公共技術中心的支持。
研究論文鏈接:https://www.pnas.org/doi/10.1073/pnas.2219419120
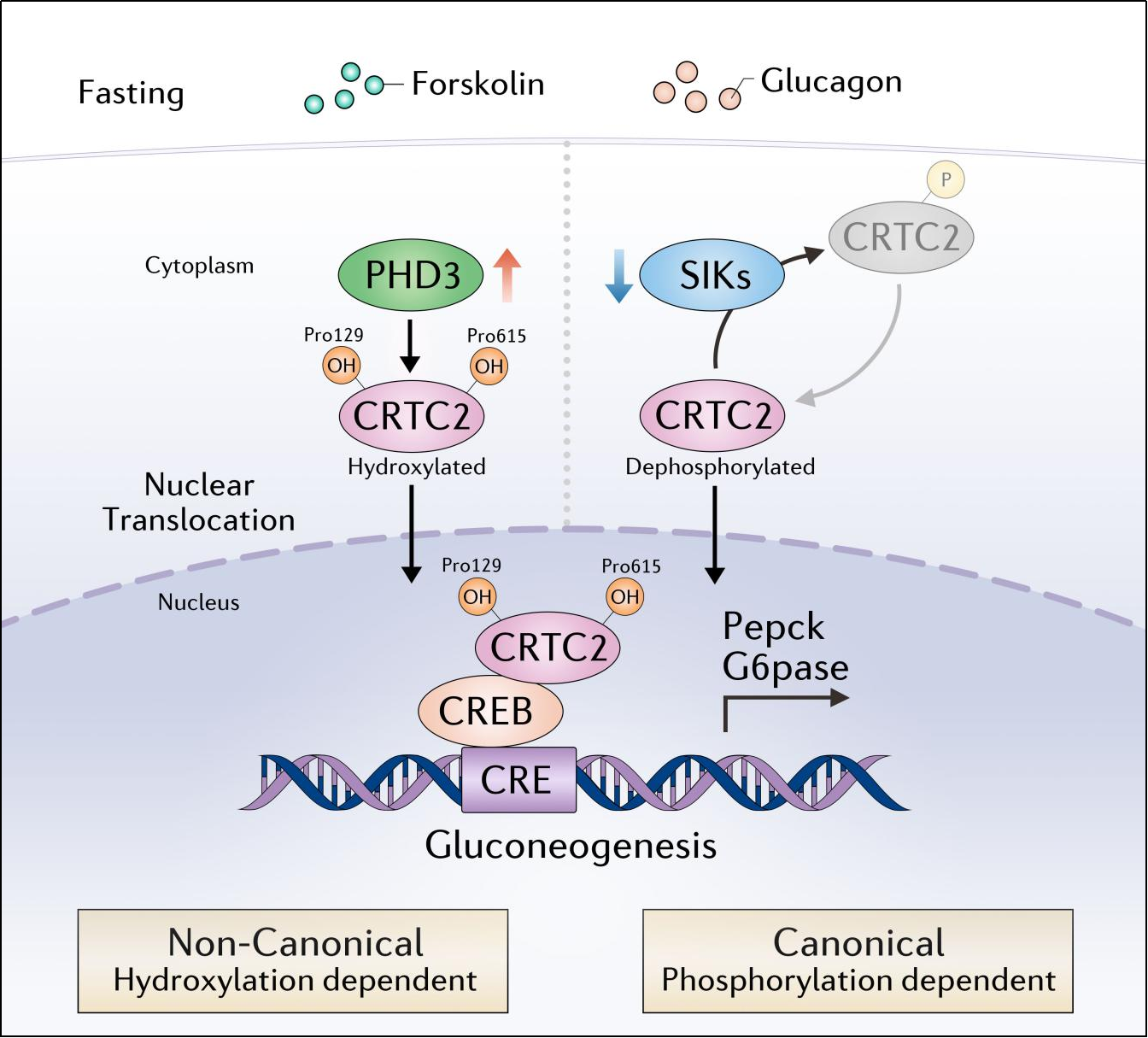
PHD3通過非經典的CRTC2羥基化修飾激活肝糖異生模式圖
在禁食或胰高血糖素刺激條件下,PHD3結合并羥基化CRTC2的Pro129和Pro615位點,導致CRTC2的核轉位和CREB/CRTC2途徑激活,促進糖異生基因表達和肝糖輸出。CRTC2羥基化是一種非經典的CRTC2翻譯后修飾,獨立于經典的CRTC2磷酸化修飾對肝臟糖異生的調控。