1月21日,中國科學院上海營養與健康研究所詹麗杏研究組合作在肝臟疾病研究領域取得重要突破,于國際學術期刊Journal of Hepatology在線發表了題為“AF6 knockout-induced upregulation of bile acid production promotes CXCL14-mediated antitumor immunity in HCC: Effect of the BA/Butyrate/CXCL14 axis in HCC”的研究成果,?揭示了膽汁酸代謝通過腸肝軸,介導新興免疫趨化因子CXCL14調控肝臟抗腫瘤免疫微環境的新機制。
研究發現,初級膽汁酸/丁酸/CXCL14 形成代謝-免疫作用軸來改善腫瘤抑制性免疫微環境,從而抑制肝癌的進展。研究首次發現了極性蛋白 AF6 是肝上皮細胞膽汁酸合成酶的核心調控子,也明確了AF6 通過調控膽汁酸代謝穩態改善肝臟抑制性免疫微環境的作用機制。這些變化表征,為未來肝癌患者的臨床治療提供了新的治療手段。
肝臟是人體的重要器官,承擔營養代謝、膽汁分泌、解毒等代謝功能,膽汁的合成和分泌是肝臟最主要的功能之一。目前尚未有直接調控肝臟膽汁酸合成的小鼠模型,因此該研究也提供了解析機體膽汁酸相關病理生理調控的動物模型,具有重要意義。
詹麗杏研究團隊既往有多項研究成果證實肝臟極性蛋白AF6與肝臟糖脂代謝密切相關。該研究首次報道了肝臟特異性敲除AF6可導致初級膽汁酸合成發生變化。通過一系列實驗,研究人員證明了肝臟 AF6 是初級膽汁酸(BA)合成的核心調節因子,可直接調節 BA 合成途徑中多種合成酶表達,特別是首步及限速酶細胞色素 P450 7A1(CYP7A1)。研究人員首先在二乙基亞硝胺(DEN)誘導的肝癌小鼠模型中,發現肝臟特異性敲除AF6可顯著抑制肝癌進展,并增強了初級BA的生成。
極性蛋白AF6在肝臟中的特異性敲除是如何抑制肝癌進展的呢?研究人員猜測可能是通過肝臟局部機制或通過腸肝軸循環機制引起。通過宏基因組、靶向代謝組學檢測等手段,研究人員進一步證明了AF6的特異性敲除導致了腸道微生物群和微生物代謝物的特征性變化,確認了是菌群代謝物丁酸的積累而非初級/次級膽汁酸的變化改變了肝腫瘤免疫微環境,這一效應是通過腸肝循環所介導。研究人員給予肝癌小鼠抗生素處理以消除腸肝軸中菌群及其代謝物帶來的影響,證實菌群清除抵消了肝臟特異性敲除AF6引起的抗腫瘤作用。通過人肝癌類器官試驗以及IHC等多種研究技術,研究人員發現丁酸能夠上調肝細胞中趨化因子CXCL14 的表達和分泌。通過進一步的單細胞測序及體外共培養試驗,研究證實肝細胞來源的CXCL14 能夠招募活化的樹突狀細胞,從而促進并增強CD8 T細胞在肝癌中的細胞毒性作用。在多種肝癌模型中,研究驗證了由腸肝循環進入肝臟的丁酸誘導的 CXCL14塑造了抑制腫瘤的免疫微環境,進而抑制了肝癌的進展。這項工作發現了不改變典型肝臟上皮完整性的情況下增強初級膽汁酸生成的小鼠模型,該模型可用于監測胃腸道中與膽汁酸相關的病理過程,包括癌癥進展。
中國科學院上海營養與健康研究所博士研究生徐珂瑩為該論文的第一作者;中國科學院上海營養與健康研究所詹麗杏研究員,江南大學醫學中心夏加增教授,南京醫科大學第一附屬醫院徐驍教授,長海醫院李兆申教授和李剛教授為文章的共同通訊作者。該工作得到了中國科學院上海營養與健康研究所周章森研究員、胡國宏研究員、呂偉研究員和李昕研究員的支持與幫助,也得到了中國科學院上海營養與健康研究所所級公共技術中心分析測試技術平臺和實驗動物技術平臺的支持。該工作獲得了科技部、國家自然科學基金委等項目的資助。
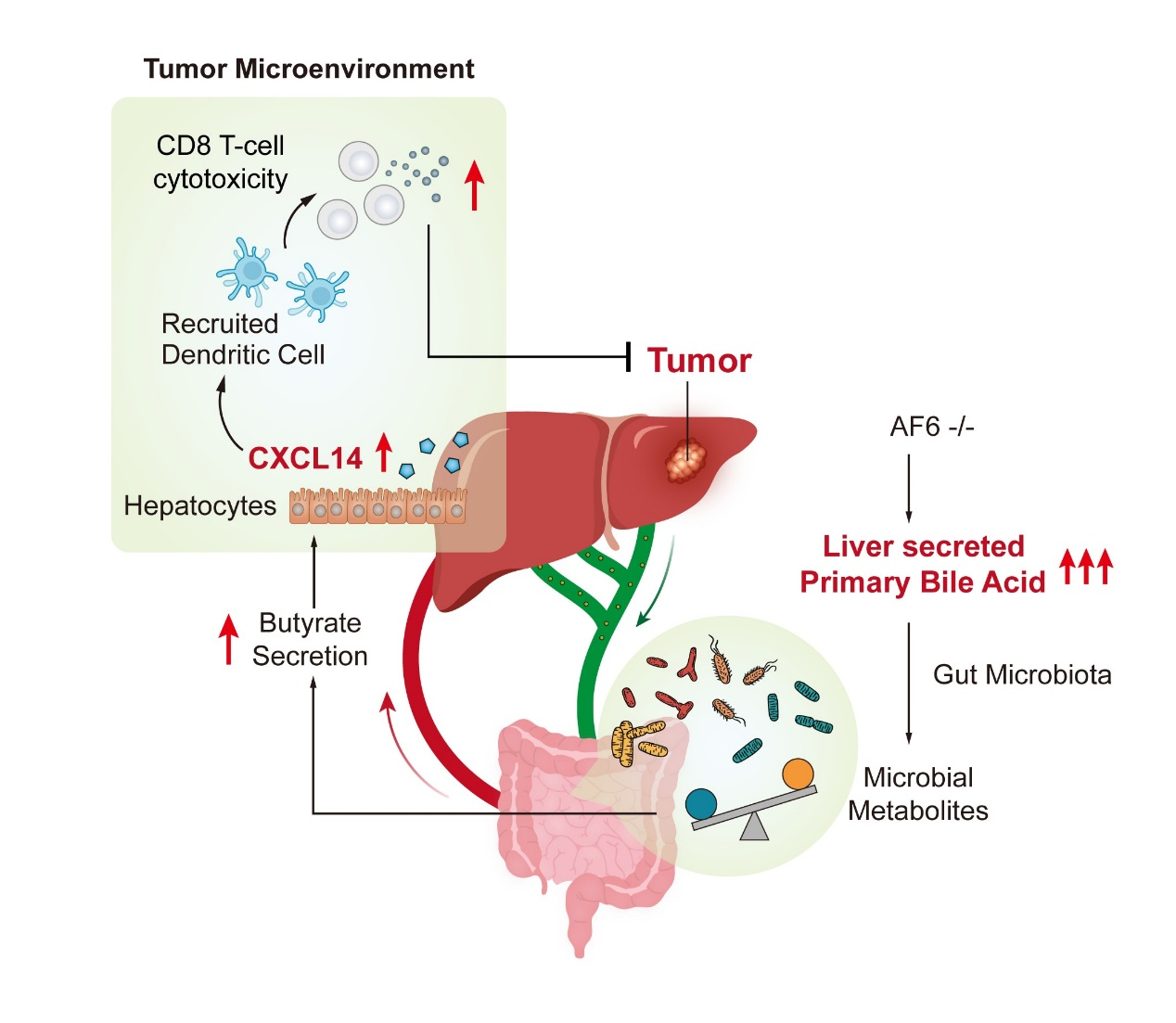
圖:肝臟AF6 誘導膽汁酸代謝-免疫作用軸增強肝癌抗腫瘤免疫的機制示意圖
論文鏈接:https://www.sciencedirect.com/science/article/pii/S0168827826000164
推送單元:詹麗杏研究組、科技規劃與任務處