8月21號,國際學術期刊The Journal of Clinical Investigation雜志在線發表了中國科學院上海生命科學研究院(人口健康領域)秦駿研究組的研究論文“Histone methyltransferase SETD2 modulates alternative splicing to inhibits intestinal tumorigenesis”。該研究揭示組蛋白H3K36三甲基化轉移酶SETD2在腸癌發生發展中的關鍵作用。研究表明SETD2的缺失影響mRNA選擇性拼接, 導致Wnt信號通路的過度激活,從而促使腸干細胞及前體細胞的惡性轉化。
組蛋白遺傳修飾酶的異常表達或功能紊亂在腫瘤發生發展中發揮重要作用。在哺乳動物細胞中,SETD2是最主要的H3K36me3修飾酶,調節基因轉錄。研究發現SETD2在腫瘤組織中存在高頻突變或缺失,尤為顯著的是在腎癌中,在其他癌癥如乳腺癌、腸癌、胃腸道間質瘤中也有報道。但目前尚未有證據闡明SETD2體內的功能。博士研究生袁懷瑞、李霓等在秦駿研究員指導下,利用遺傳小鼠模型和病人數據驗證,揭示SETD2缺失可以協同Wnt信號活化促進腸癌的發生發展。在正常腸道干細胞中,Wnt信號通路被控制在合理的閾值,既維持了干細胞自我更新及增殖,同時保證腸干細胞終末分化。腫瘤中SETD2的缺失打破了Wnt信號在腸道干性維持及終末分化間的平衡,導致腺窩底部干細胞快速增生形成癌前組織。機制研究表明其通過影響Gene body區H3K36me3的水平,調控眾多與腫瘤相關基因RNA的選擇性拼接。SETD2的下降,造成Wnt信號關鍵調節基因DVL2的 intron retention減少,從而避免DVL2的NMD,最終過度激活Wnt信號通路,導致腸干細胞及前體細胞的惡性轉化。鑒于SETD2具有酶活,存在小分子藥物靶向的可能性,因此本項目的完成將可能對于腸癌的治療提供新的策略。同時SETD2調控機制的解析也將有助于我們在表觀調控層面對于腸癌發生發展進一步了解。
該研究得到了來自上海市第十人民醫院符達教授,上海交通大學李力教授,上海市腫瘤醫院彭俊杰教授,南京醫科大學王曉明教授,四川大學李沁桐等大力幫助,并得到了國家自然科學基金委、科技部,以及中科院等科研項目的資助以及上海生科院(人口健康領域)公共技術平臺以及動物平臺的支持。
原文鏈接:https://doi.org/10.1172/jci94292
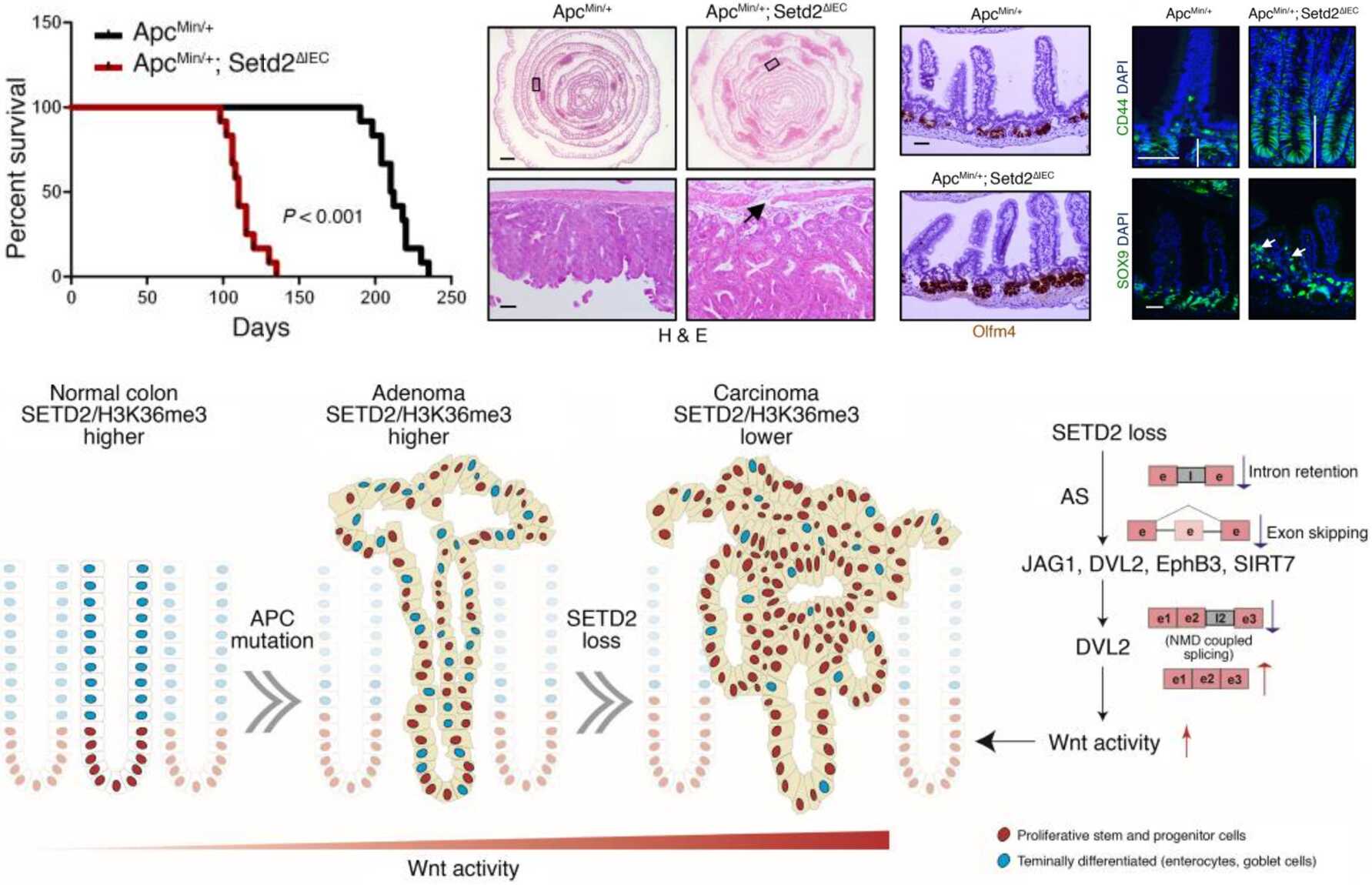
圖示:SETD2在腸癌發生發展中的功能及調控機制