11月24日,國際著名學術期刊Science發表了中國科學院上海生命科學研究院(人口健康領域)計算生物學伙伴研究所楊力研究員與中國科學院上海生物化學與細胞生物學研究所陳玲玲研究員合作的題為“Enhancing the RNA engineering toolkit”的perspective文章,對在當期Science和近期在Nature上發表的兩項獨立研究工作進行了點評和推薦。
RNA水平的基因表達調控與生物體正常生理功能息息相關,其異常變化則導致多種重要人類疾病的發生, 但是對RNA的改造操作手段則比較匱乏。來自Broad研究所的Feng Zhang教授研究組首先在Nature上報道了class 2 type VI CRISPR-Cas-Cas13a可對RNA分子進行靶向切割,進而實現 RNA水平抑制基因表達的功能;而RNase失活改造的dCas13a則可以用于追蹤內源RNA分子的細胞定位研究等。在當期Science,Feng Zhang教授研究組進一步篩選了多種class 2 type VI CRISPR-Cas系統(包括Cas13a、Cas13b和Cas13c),展示了來自Prevotella sp.的Cas13b(PspCas13b)具有最優的RNA靶向切割效應,其比RNAi系統具有更好的專一性和更低的脫靶效應;研究人員進一步將RNase失活改造的dCas13b與A-to-I RNA編輯酶ADAR偶聯(REPAIR系統),實現了在RNA水平上的A-to-I/G單堿基編輯(base editing)。來自Harvard大學的David Liu教授研究組在2016和2017年分別報道了DNA水平的C-to-T 和A-to-G單堿基編輯。相對于DNA水平的單堿基編輯,RNA水平的單堿基編輯避免了任何由于對遺傳基因組DNA操作所引發的脫靶效應的擔憂。由于RNA在細胞內的豐度和結構都千差萬別,REPAIR系統介導的RNA單堿基編輯會因RNA不同而異。當然,DNA和RNA水平的單堿基編輯為基因編輯改造以治療疾病又提供了多種可供選擇的高效手段。
陳玲玲研究員和楊力研究員利用計算和實驗相結合的方法,長期從事RNA組學、非編碼RNA和RNA編輯研究。 從環形長非編碼RNA(Zhang et al, Mol Cell 2013;?Zhang et al, Cell 2014;?Zhang et al, Genome Res 2016;?Li et al, Mol Cell 2017),特殊類型長非編碼RNA(Yin et al, Mol Cell 2012;?Zhang et al, BMC Genomics 2014;?Wu et al, Mol Cell 2016;?Xing et al, Cell 2017)和RNA編輯修飾(Zhu et al, BMC Genomics 2013;?Chen et al, Cell Res 2015;?Xiang et al, Mol Cell in press)等領域揭示了基因表達在轉錄/轉錄后水平的復雜性和多樣性,為深入研究RNA水平的復雜性調控提供了重要的理論基礎。
原文鏈接:https://doi.org/10.1126/science.aar2400
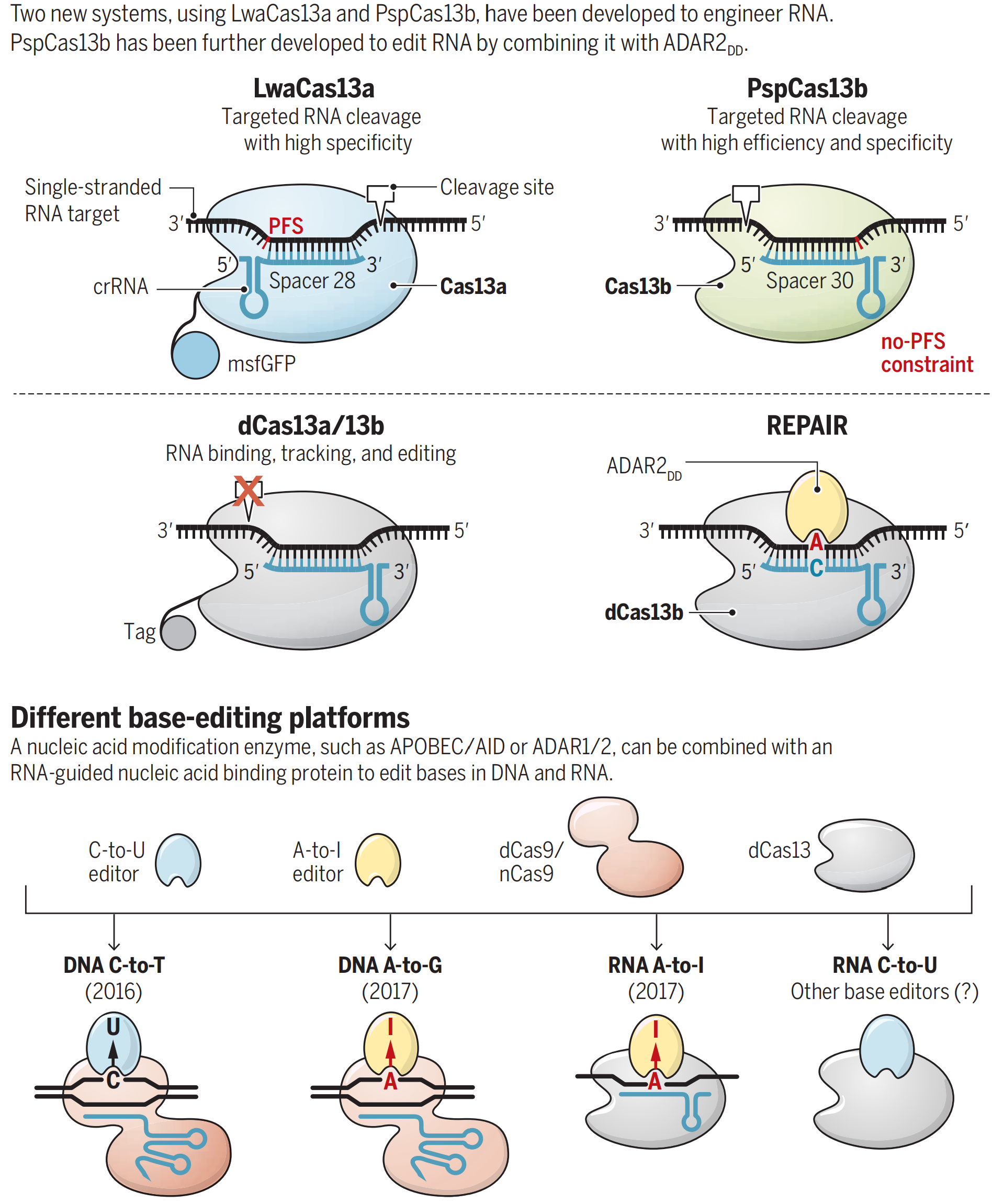
圖示:Cas13介導的RNA操作新體系