近日,中國科學院-馬普計算生物學研究所楊力研究組與上海科技大學生命學院陳佳研究組和黃行許研究組通過合作研究,開發出一系列基于CRISPR/Cpf1(Cas12a)的新型堿基編輯器(dCpf1-BE),相關成果以“Base editing with a Cpf1– cytidine deaminase fusion”為題,在線發表在國際知名學術期刊《自然-生物技術》(Nature Biotechnology)上。
傳統的CRISPR/Cas9基因編輯技術雖然具有較高的基因敲除效率,但在執行特定的堿基替換(譬如對造成遺傳性疾病的點突變進行矯正)時效率通常很低,這極大地限制了CRISPR/Cas9基因編輯的應用。近期,利用CRISPR/Cas9和APOBEC(胞嘧啶脫氨酶)整合而發展出的新型堿基編輯系統(Base Editor, BE),可在單堿基水平(如胞嘧啶向胸腺嘧啶)實現高效率的基因組靶向編輯改造。這種新型堿基編輯系統理論上可對數百種引起人類疾病的基因組點突變進行定點矯正,因此擁有巨大的臨床應用潛力。目前已報道的堿基編輯系統均是利用Cas9蛋白(主要是Streptococcus pyogenes?Cas9, SpCas9和Staphylococcus aureus Cas9, SaCas9)執行與基因組的靶向性結合,而這種靶向性結合依賴于靶點旁側的PAM(Protospacer Adjacent Motif)序列。SpCas9和SaCas9蛋白所識別的PAM序列多含鳥嘌呤/胞嘧啶(G/C-rich),因此利用已報導的堿基編輯系統無法在腺嘌呤/胸腺嘧啶富集(A/T-rich)區域進行高效的堿基編輯操作。
在這項最新的研究中,科研人員構建了一系列基于CRISPR/Cpf1蛋白的新型堿基編輯器(dCpf1-BE)。由于Cpf1蛋白可識別富含腺嘌呤/胸腺嘧啶的PAM序列,這種基于Cpf1的新型堿基編輯器實現了在腺嘌呤/胸腺嘧啶富集區域的堿基編輯操作。在拓展了可編輯區域的同時,基于Cpf1的新型堿基編輯器所產生的編輯副產物也較低,因此具有更高的編輯精準度。這種基于Cpf1的新型堿基編輯器與現有的基于Cas9的堿基編輯器可實現堿基編輯的有效互補,為堿基編輯系統在基礎研究及未來臨床領域的全面深入應用提供了新方法、拓展了新思路。
楊力研究員長期從事計算生物學和組學研究。在此項最新的合作研究中,利用計算和實驗相結合的高通量體系,成功開發出一系列基于 Cpf1的新型堿基編輯器系統,實現了在腺嘌呤/胸腺嘧啶富集區域的堿基編輯操作。在與陳佳教授前期的一系列合作研究中,闡明了APOBEC在CRISPR/Cas9引起的基因組DNA斷裂修復過程中產生突變的分子機制(Lei et al., Nature Structural & Molecular Biology 2018)并成功合作開發出了增強型的基因組堿基編輯系統(Wang et al., Cell Research 2017)。
該工作在楊力研究員、陳佳教授、黃行許教授的共同指導下,由陳佳研究組2014級碩博連讀研究生李瀟颯、楊力研究組2015級碩博連讀研究生王瀅和黃行許研究組2014級碩博連讀研究生劉亞京等共同完成。該項研究得到了國家自然科學基金委、科技部、上海市科委和上科大科研啟動基金的支持。該研究使用的高通量測序數據由PICB Omics Core完成,并儲存于NCBI (GEO:?GSE110136)和PICB大數據中心(National Omics Data Encyclopedia:?NODEP00371765)。
原文鏈接:https://doi.org/10.1038/nbt.4102
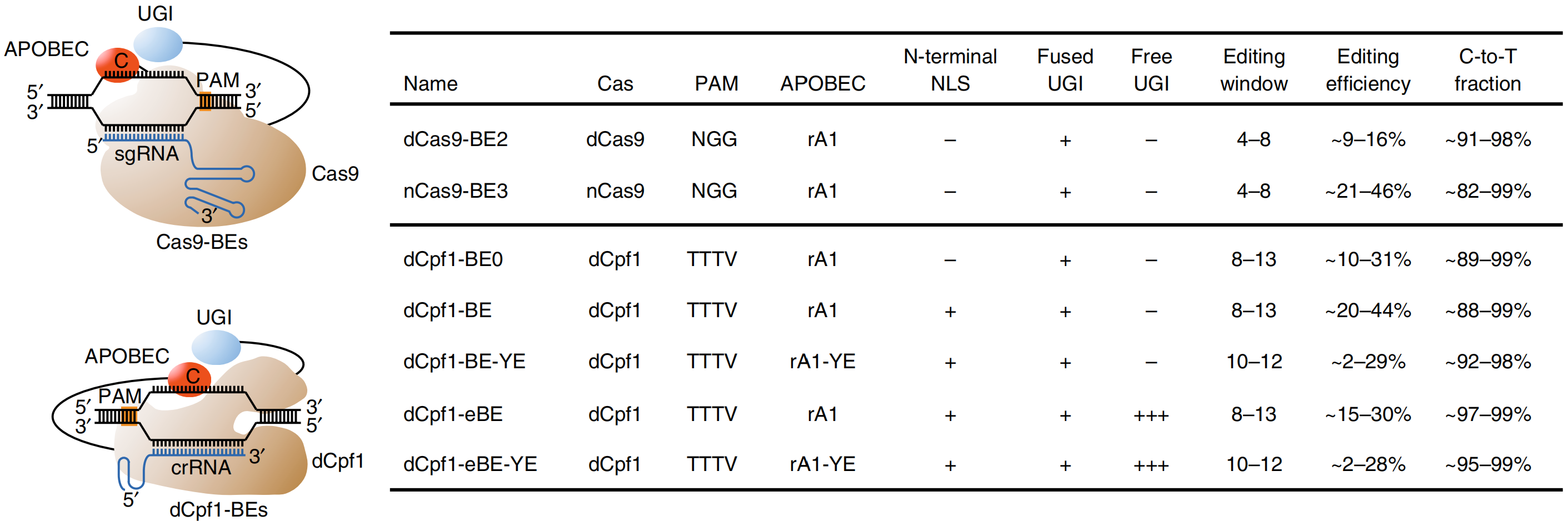
Cas9堿基編輯器與Cpf1堿基編輯器的特點比較