5月11日,國際學術期刊PLoS?Biology在線發表了中國科學院上海營養與健康研究院(暫名)應浩研究組的最新研究成果“Metabolic benefits of inhibition of p38α in white adipose tissue in obesity”。該研究發現促分裂原活化蛋白激酶(MAPK)家族成員p38α通過影響PKA/CREB/UCP-1信號通路,調控白色脂肪組織的米色化過程并進一步影響能量代謝的狀態。
褐色脂肪中線粒體含量豐富,解偶聯蛋白UCP1高表達,對機體的能量代謝和產熱活動至關重要。在低溫刺激條件下,小鼠皮下白色脂肪中會出現米色脂肪細胞(beige adipocytes),即白色脂肪的米色化過程。米色脂肪細胞具有褐色脂肪類似的產熱功能,可促進能量消耗。白色脂肪米色化后,能量代謝增加,對整個機體的代謝有改善作用,并且能夠抵抗高脂飲食誘導的肥胖形成。
p38是MAPK家族成員中重要的應激激活蛋白,屬于絲氨酸/蘇氨酸激酶。p38的磷酸化激活主要通過MAP3K/MKK/MAPK的三級激酶鏈連鎖反應,其激活位點的去磷酸化主要通過磷酸酶來進行。p38包括α,β,γ和δ四種亞型,各自的分布具有組織特異性。其中,p38α在全身各組織廣泛表達,是肝臟、脂肪等組織表達的主要亞型。應浩課題組的前期研究發現,在肝臟中p38α能夠調控糖異生過程(Jing Y, Liu W and et al. Journal of Hepatology 2014)。但是在脂肪中,p38α對能量代謝的作用并未得到系統的研究。
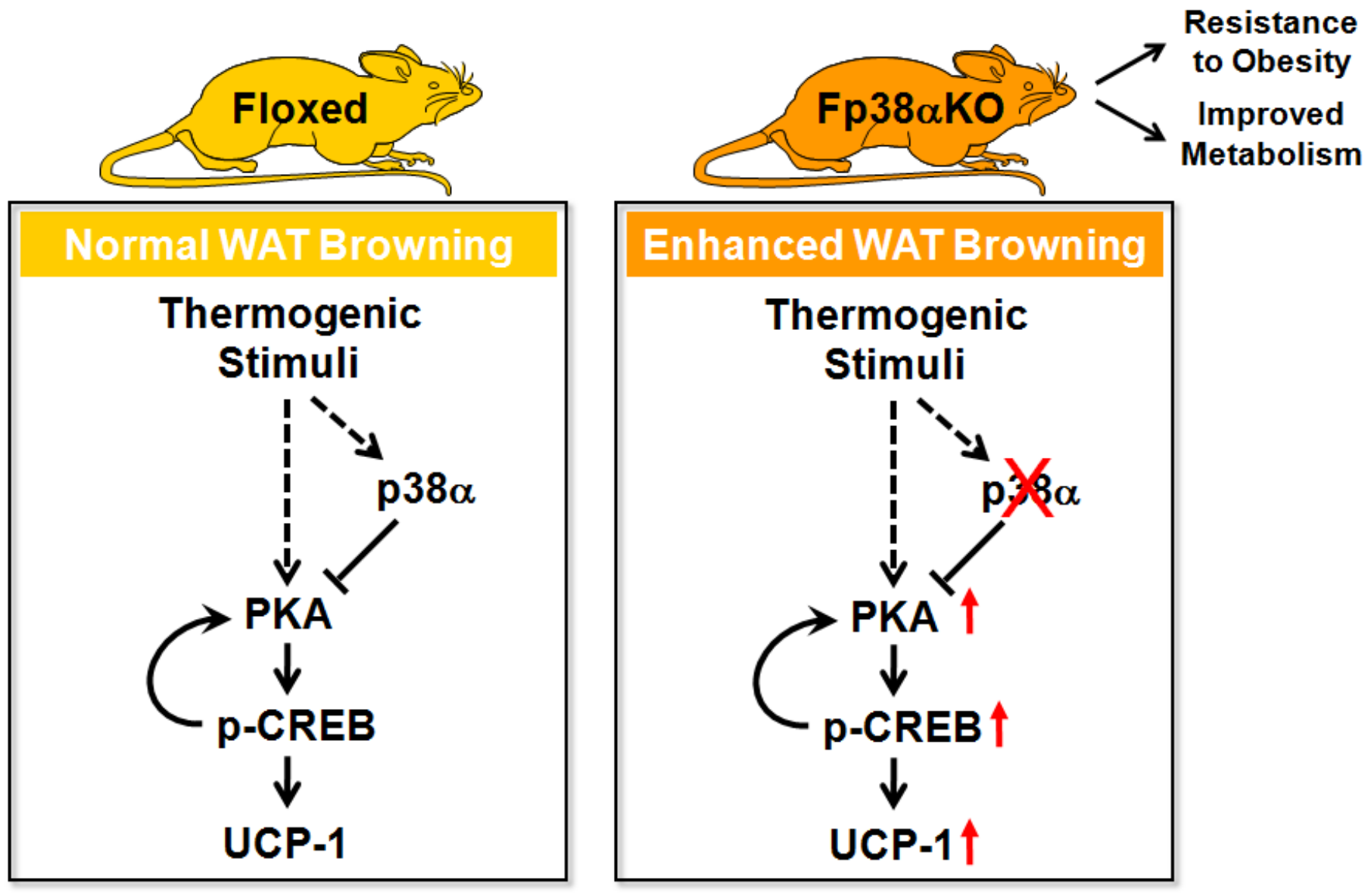
在這項最新的研究中,博士研究生張圣潔等人在應浩研究員的指導下,發現脂肪組織特異敲除p38α后小鼠的體重減輕,但是體溫維持能力以及褐色脂肪產熱功能基本不受影響。而在低溫環境下,白色脂肪p38α缺失后能夠觀察到米色脂肪細胞比對照明顯增多,米色化活動加劇。在β腎上腺素受體激動劑CL316,243的刺激下,脂肪組織p38α缺失的小鼠能量消耗顯著增加。通過基因敲除小鼠和抑制劑定點注射兩種手段,發現p38α缺失或活性受損后能夠抵抗高脂飲食誘導的肥胖以及db/db小鼠體重的上升。通過一系列體外水平實驗,發現p38α缺失后在白色脂肪細胞中PKA以及CREB的活性同時上調,促進UCP1的轉錄表達,細胞的米色化進程加快,能量消耗增加。
該研究首次闡明了p38α在白色脂肪米色化過程中的功能,進一步揭示了白色脂肪細胞米色化的具體機制。為將脂肪組織p38α作為靶點,研發治療肥胖等代謝性疾病的藥物提供了理論依據。
該研究得到了中國科學院上海營養與健康研究院(暫名)技術平臺、中國科學院上海藥物所黃銳敏研究員和彭程遠老師以及中國科學院上海有機化學研究所的湯文軍研究員的大力支持和幫助。該研究得到國家科技部(2016YFA0500102,2016YFC1304905),國家基金委(31525012,,31600954,,31371189,,81570768, 81471016),以及中科院科研基金(XDA12040324,XDA12020108)的支持。
原文鏈接:https://doi.org/10.1371/journal.pbio.2004225