2018年6月26日,國際知名學術期刊《免疫》在線發(fā)表了中國科學院上海生命科學研究院(營養(yǎng)與健康院)常興研究組題為“Iron drives T helper cells pathogenicity by promoting RNA-binding protein PCBP1- mediated proinflammatory cytokine production”的最新研究成果,發(fā)現了輔助性T細胞中鐵代謝通過調控促炎性細胞因子表達參與自身免疫疾病,并證明RNA結合蛋白PCBP1介導的轉錄后調控途徑為連接鐵代謝與細胞因子表達的調控的橋梁。
自身免疫性疾病是人體的免疫系統錯誤地識別自身器官、組織和細胞,誘導免疫應答,繼而造成自身損傷的一類疾病。大多數自身免疫疾病的發(fā)病機制至今還不完全明確,缺乏完全治愈的有效治療手段。臨床研究發(fā)現,自身免疫疾病發(fā)病的原位組織存在鐵離子的過量沉積,如多樣性硬化病人的腦組織和風濕性關節(jié)炎病人的關節(jié)滑液等。但是,鐵離子沉積對疾病的發(fā)展和功能仍然不清楚。
博士后王志章等研究人員發(fā)現,多種方法改變T細胞中鐵離子含量,會選擇性調控促炎性細胞因子GM-CSF的表達,并在多樣性硬化小鼠模型EAE中影響疾病的發(fā)生。進一步通過shRNA篩選,發(fā)現具有鐵離子伴侶功能的RNA結合蛋白PCBP1可能參與該過程。T細胞中PCBP1缺陷與鐵離子缺陷類似,可以抑制GM-CSF的表達和EAE發(fā)生。更進一步的機制研究發(fā)現,PCBP1直接結合mRNA 3'UTR中富含UC的序列,促進GM-CSF等mRNA的穩(wěn)定性和表達;而鐵離子保護PCBP1蛋白不被Caspase剪切降解,提示PCBP1可以作為胞內鐵離子的傳感器,調控免疫細胞轉錄組的動態(tài)變化和致病性。
該研究鑒定出調控GM-CSF表達的新的順式作用元件,及其相關的反式作用因子PCBP1,揭示了GM-CSF新的轉錄后調控機制;同時豐富了代謝環(huán)境通過RNA結合蛋白轉錄后調控基因表達的模型;闡釋了鐵代謝異常促進自身免疫疾病的機制,為多發(fā)性硬化等自身免疫疾病的治療提供的新的靶點和思路。
該工作得到了科技部、國家自然科學基金委、和上海市科委的相關資助。
原文鏈接:https://doi.org/10.1016/j.immuni.2018.05.008
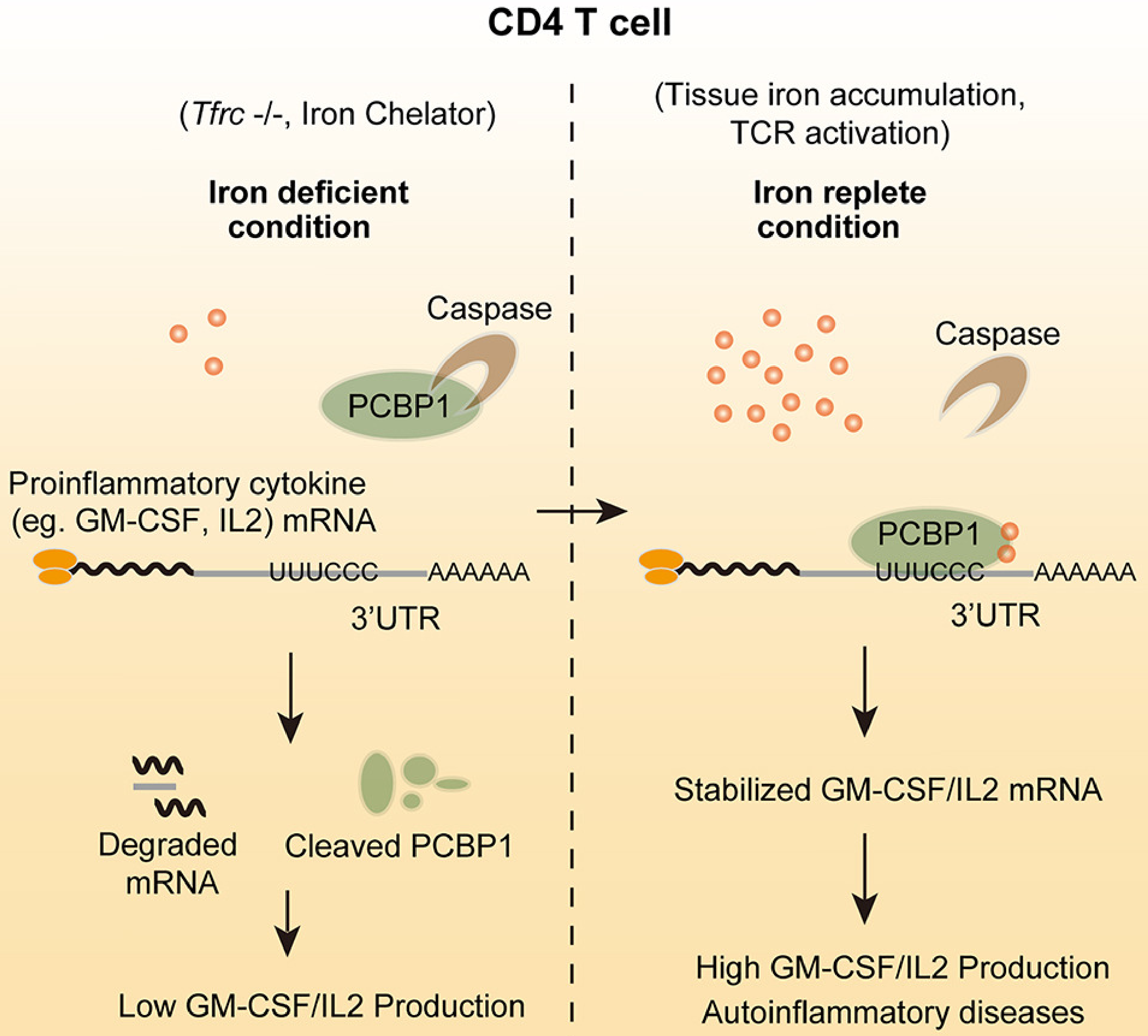
圖.T細胞中“鐵離子-PCBP1-細胞因子”調控模型
在輔助性T細胞中,胞內鐵離子充足時,PCBP1蛋白穩(wěn)定表達,GM-CSF等促炎性細胞因子mRNA半衰期延長,從而大量產生細胞因子;胞內鐵離子匱乏時,PCBP1被Caspase剪切降解,GM-CSF等促炎性細胞因子mRNA半衰期縮短,快速降解,從而使細胞因子產生受損。