2019年5月24日,國際學術期刊Diabetes在線發表了中國科學院上海營養與健康研究所詹麗杏研究組的研究成果“Polarity Protein AF6 Controls Hepatic Glucose Homeostasis and Insulin Sensitivity by Modulating IRS1/AKT Insulin Pathway in an SHP2-dependent Manner”。該研究發現極性蛋白AF6(afadin and MLLT4)能夠通過結合酪氨酸磷酸酶SHP2并且上調SHP2的活性從抑制IRS1/AKT通路,并證明糖尿病小鼠肝臟中敲減AF6蛋白表達可以有效提高胰島素敏感性并緩解胰島素抵抗。
2型糖尿病(Type 2 diabetes, T2D)是一種慢性非傳染性疾病。快速城市化、不健康的飲食和日益久坐的生活方式造成T2D的發病率不斷升高。T2D表現為胰島素抵抗和高血糖,但迄今為止其發病機制尚未完全闡明。肝臟是機體重要的代謝器官,在維持血糖穩態中發揮重要作用。肝臟糖代謝紊亂參與T2D的發生發展。深入了解肝臟糖代謝調控的分子機制不僅有助于揭示2型糖尿病發生發展的致病機理,而且能為該病的治療提供新的靶標和思路。
極性蛋白AF6,又叫afadin或者MLLT4,是一種在進化上非常保守的F-actin結合蛋白,在胚胎和成人幾乎所有的組織中都有表達。AF6在神經系統的發育、細胞極性的建立和維持、細胞的增殖和分化、腫瘤的發生發展等多種過程中都發揮著重要的作用,但是AF6在肝臟中的功能,以及AF6是否參與細胞代謝都知之甚少。
博士研究生戴騁等人在詹麗杏研究員的指導下,探討了極性蛋白AF6調控血糖穩態和胰島素敏感性的新功能及作用機制。該研究發現高脂飲食誘導和db/db小鼠這兩種糖尿病模型小鼠的肝臟中AF6的表達均顯著提高。研究組進一步構建了AF6肝臟特異性敲除小鼠(AF6 LKO),證明AF6 LKO小鼠其血糖水平、葡萄糖耐受性、胰島素敏感性均有顯著改善。在肝原代細胞中發現,酪氨酸磷酸酶Src homology 2 domain-containing phosphatase 2(SHP2)是AF6的作用靶點,顯示AF6結合SHP2并促進其磷酸酶活性是肝臟胰島素信號通路的重要抑制信號。另一方面,SHP2的過表達有效阻斷AF6敲除引起的胰島素通路的活化以及小鼠的血糖表型,說明AF6能夠通過SHP2來抑制IRS1/AKT信號通路。體內體外實驗均證明了肝臟過表達AF6能夠抑制胰島素通路重要成員IRS1,以及AKT和GSK3β等下游信號,由此我們確認了AF6過負荷與肝臟胰島素信號通路抑制相關分子機制。最后,在高脂飲食誘導的糖尿病小鼠和db/db小鼠肝臟中下調AF6能夠顯著改善高血糖和胰島素抵抗的癥狀。該研究發現了肝臟中極性蛋白AF6調控糖代謝穩態和胰島素敏感性的新功能和調控機制,為T2D的治療提供了新的思路,具有重要的理論意義和潛在的應用價值。
該研究得到了中國科學院上海營養與健康研究所樂穎影研究員和武漢大學劉勇教授的支持和幫助。該項目得到了國家科技部、國家自然科學基金委以及中科院藥物先導等項目的共同資助以及上海營養與健康研究所公共技術平臺的支持。
原文鏈接:https://doi.org/10.2337/db18-0695
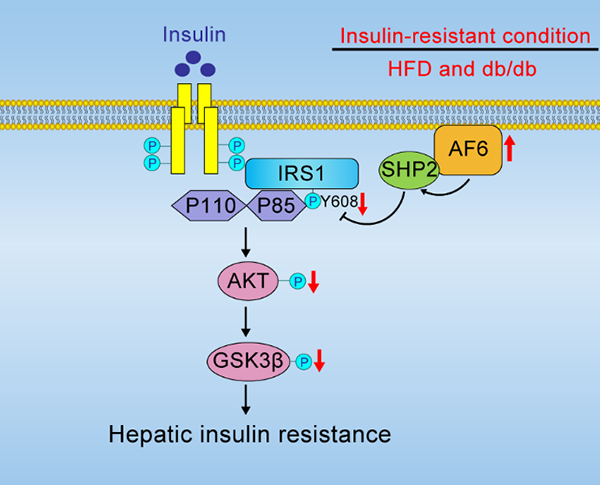
調控胰島素敏感性的工作機制