2019年9月7日,中國科學院上海營養與健康研究所孫宇組在Aging Cell雜志上發表了題為“Targeting amphiregulin (AREG) derived from senescent stromal cells diminishes cancer resistance and averts programmed cell death 1 ligand (PD‐L1)-mediated immunosuppression”的論文。該研究發現,人源基質細胞在化療過程中會被動進入衰老狀態,發展為典型SASP的同時生成與釋放一種名為AREG (amphiregulin,雙向調節素)的外泌因子,持續不斷地進入受損的微環境空間。AREG一方面促進病灶中殘存癌細胞惡性表型并導致其獲得耐藥性,從而造成臨床治療抵抗;另一方面誘導癌細胞上調表達PD-L1,形成免疫抑制性微環境,使得癌細胞逃逸免疫監控。此外,外周血中AREG可通過常規技術實時檢測,其含量的動態變化同患者生存密切相關,可作為將來臨床預后與療效評價的一個精確指標。
AREG作為一種生長因子可以參與調控多種生理過程,包括乳腺導管、卵母細胞、胚囊和骨組織的發育和成熟等。已有報道AREG廣泛表達于多種腫瘤組織,包括乳腺癌、肺癌、結直腸癌、卵巢癌、前列腺癌及胰腺癌等,具有顯著促癌活性。在一些特殊場合,AREG可參與調控免疫抑制過程,如炎癥條件下的Foxp3+ Treg cell表達EGFR,而AREG體外可以顯著提高Treg cell的功能;在colitis和腫瘤免疫模型中mast cell衍生的AREG可以徹底恢復Treg cell的活性,靶向這一免疫調控機制有可能促進那些靶向癌癥病人體內EGFR為治療依據的成功率。
研究人員發現相比于同器官來源的上皮癌細胞,以成纖維細胞為主要成分的基質組織在基因毒藥物作用下更加顯著地合成與外泌AREG。其轉錄和翻譯均呈時間依賴性,即在細胞進入深度衰老階段后方達到高峰期。該SASP因子在多個人源基質細胞系中的表達十分類似,即在多組織、多器官中均具脅迫響應性。體外數據表明,衰老基質細胞通過激活轉錄因子NF-κB結合到AREG基因的啟動子區域,增強AREG的轉錄,從而上調表達AREG。衰老基質細胞來源的AREG能夠結合并活化前列腺癌細胞表面受體EGFR,進而激活下游促癌信號通路Akt-mTOR和Mek-Erk并磷酸化Stat3。通過在基質細胞中過表達或敲除AREG,發現基質細胞來源的AREG顯著促進癌細胞的增殖率、遷移率和侵襲性。更重要的,基質AREG造成上皮癌細胞出現顯著耐藥性,其劑量反應曲線出現明顯的平行漂移。此外,基質AREG促進上皮癌細胞表達PD-L1,造成癌細胞免疫逃逸,敲除PD-L1能夠有效促進免疫細胞對癌細胞殺傷作用。
動物實驗中,以MIT為主的化療藥物可以造成癌細胞的終端體積顯著下降;但在基質細胞同時存在的情況下,腫瘤滯留體積卻大幅上升,暗示微環境在治療過程中賦予殘存癌細胞顯著的耐藥性。化療藥物給藥荷瘤小鼠的過程中,一些SASP典型外泌因子如IL6、IL8、WNT16B、SFRP2的表達均出現上調,暗示體內條件下細胞衰老和SASP的出現。研究人員注射人源PBMC并重構了免疫完整型小鼠(Rag2-/-IL-2Rγnull),發現MIT協同PD-L1/PD-1阻斷劑給藥可以進一步縮小腫瘤終端體積,暗示微環境中的AREG同時能夠賦予癌細胞免疫逃逸的能力。
該研究的亮點在于第一次揭示腫瘤微環境內的基質細胞在化療過程中可以生成與釋放大量的SASP因子,其中的AREG可以激活療后階段殘存下來的癌細胞,使其獲得對于臨床藥物的抵抗;同時,AREG塑造了臨床背景下的免疫抑制性微環境,從而使得癌細胞能夠逃脫細胞毒T細胞、巨噬細胞等免疫亞群的攻擊。這種獲得性耐藥和免疫逃逸,正是造成日后腫瘤復發和轉移的病理基礎。
博士生許奇霞和復旦大學中山醫院泌尿外科龍啟來為該文共同第一作者,孫宇研究員為通訊作者。該研究得到了美國Buck衰老研究所Judith Campisi教授等人的幫助,相關工作在科技部、自然科學基金委等國家機構的共同資助以及上海營養與健康研究所公共技術平臺的支持下完成。
原文鏈接:https://onlinelibrary.wiley.com/doi/full/10.1111/acel.13027
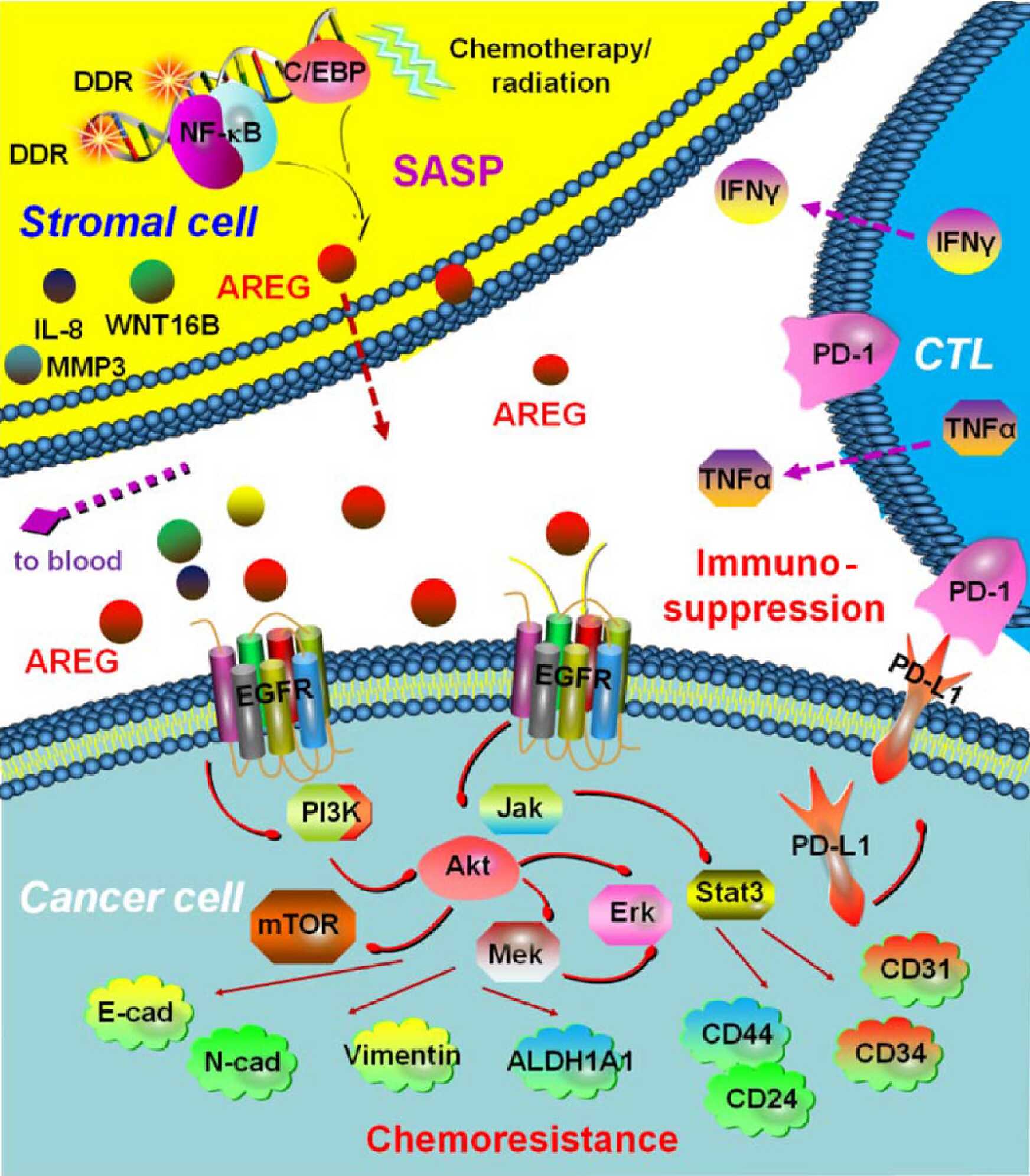
圖注:微環境中的基質細胞在化療損傷背景下進入衰老狀態并合成、釋放SASP外泌因子AREG,導致癌細胞獲得性耐藥并形成免疫抑制性微環境,最終加速疾病惡化進程。