2019年9月13日,國際學術(shù)期刊Nature Communications在線發(fā)表了中國科學院營養(yǎng)與健康研究所章海兵研究組的最新研究成果“Ubiquitination of RIPK1 suppresses programmed cell death by regulating RIPK1 kinase activation during embryogenesis”。該研究揭示了重要激酶蛋白RIPK1通過K376位點的泛素化修飾,調(diào)控細胞生存與死亡命運轉(zhuǎn)換的關(guān)鍵分子機制,為相關(guān)疾病的治療提供了新的思路。
細胞死亡是多細胞生物體維持自身穩(wěn)態(tài)與正常發(fā)育的基本生命活動,人類多數(shù)疾病從根本上說歸因于細胞死亡異常(過多或過少)。RIPK1蛋白是調(diào)控細胞凋亡、細胞程序性壞死以及炎癥信號通路中的關(guān)鍵分子,參與胚胎發(fā)育、造血系統(tǒng)發(fā)育以及免疫穩(wěn)態(tài)維持等多種重要生物學過程,最近有報道發(fā)現(xiàn)RIPK1基因突變的病人同時表現(xiàn)自身免疫缺陷及自身炎癥性疾病,提示RIPK1在人體免疫調(diào)控中具有關(guān)鍵作用,而且靶向RIPK1的小分子藥物治療漸凍癥、風濕性關(guān)節(jié)炎以及結(jié)腸炎等疾病也在臨床試驗階段。分子機理研究顯示,RIPK1一方面通過參與介導NF-kB及MAPK信號通路促進細胞存活及炎癥反應(yīng),另一方面RIPK1可以通過與FADD、Caspase8等分子互作介導細胞凋亡,而當?shù)蛲鐾繁灰种茣r,RIPK1可以通過與RIPK3結(jié)合形成壞死小體,激活下游MLKL誘導細胞程序性壞死的發(fā)生。而目前對RIPK1在不同應(yīng)激條件下如何通過轉(zhuǎn)換不同的信號通路而決定細胞存活或死亡,這個關(guān)鍵的生死轉(zhuǎn)換的分子機制仍不清楚。
章海兵研究組的研究人員發(fā)現(xiàn)RIPK1的一個主要的泛素化位點Lys376的泛素化修飾是決定細胞命運的關(guān)鍵。Lys376是RIPK1蛋白上的重要泛素連接位點,可以通過連接K63泛素鏈招募下游IKK復(fù)合體,從而激活NF-kB信號通路。利用CRISPR-Cas9基因編輯系統(tǒng),研究人員構(gòu)建了RIPK1 K376R位點突變的小鼠,并意外地發(fā)現(xiàn)純合突變的小鼠在胚胎發(fā)育至12.5天時死亡。研究人員進一步發(fā)現(xiàn),從突變小鼠胚胎分離的成纖維細胞對于TNF-a介導的細胞凋亡和細胞壞死表現(xiàn)出較野生型細胞更強的敏感性,而RIPK1的激酶抑制劑Necrostatin-1能夠有效抑制突變細胞的過度死亡。因此,該突變引起的小鼠胚胎致死可能是過度激活了RIP1激酶活性依賴的細胞凋亡和細胞壞死。為了在體內(nèi)驗證這一推測,研究人員對突變小鼠進行了藥物干預(yù),發(fā)現(xiàn)Necstatin-1能夠有效延遲小鼠的胚胎期死亡。而在突變小鼠的背景下同時敲除介導細胞凋亡的蛋白FADD和介導細胞壞死的蛋白RIPK3或MLKL能夠使突變小鼠存活至成年。而當小鼠僅攜帶一半劑量的突變基因時,該小鼠也能夠存活至成年。這些結(jié)果說明,在胚胎正常發(fā)育過程中,Lys376介導的RIPK1泛素化能夠“關(guān)閉”RIPK1的激酶活性,從而抑制細胞異常的細胞凋亡和程序性壞死,保證胚胎的正常發(fā)育。此外,研究人員發(fā)現(xiàn)在突變小鼠的基礎(chǔ)上敲除TNFR1也能夠阻止突變小鼠的胚胎致死,但是該雙突變小鼠在出生后兩周內(nèi)會發(fā)生嚴重的系統(tǒng)性炎癥。研究人員意外地發(fā)現(xiàn)這種嚴重的系統(tǒng)性炎癥是依賴于RIPK3的,敲除RIPK3可以顯著抑制這種系統(tǒng)性炎癥疾病的發(fā)生。這些結(jié)果說明,在小鼠出生后,Lys376介導的RIPK1泛素化能夠抑制RIPK3依賴的系統(tǒng)性炎癥。綜上所述,該研究通過對RIPK1 Lys376位點體內(nèi)功能的研究,闡明了這一重要位點通過調(diào)控RIPK1的激活介導的細胞死亡及炎癥信號通路,從而調(diào)控胚胎發(fā)育和炎癥性疾病的分子機制,為今后探究RIPK1的泛素化修飾在相關(guān)疾病中的作用以及尋找潛在藥物靶點提供了新的思路。值得關(guān)注的是,《Nature Communications》同期在線發(fā)表了清華大學林欣教授研究組關(guān)于RIPK1調(diào)控相同結(jié)論的研究論文。
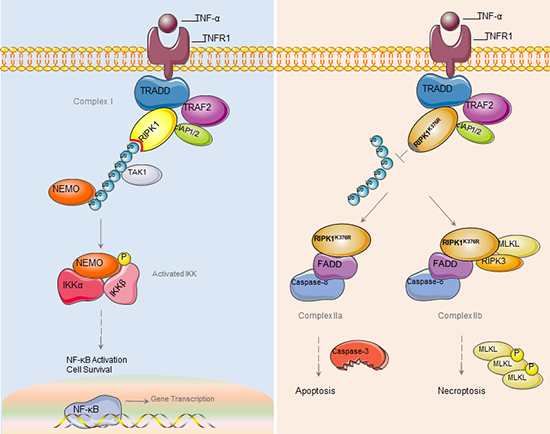
RIPK1 K376泛素化調(diào)控死亡與炎癥的分子機制
中國科學院上海營養(yǎng)與健康研究所的章海兵研究員為文章的通訊作者,研究組的博士研究生張希希和張海威為文章的共同第一作者。本研究得到了中國科學院生物化學與細胞生物學研究所周斌研究員,上海巴斯德研究所王海坤研究員,華東師范大學李大力教授,上海營養(yǎng)與健康研究所丁秋蓉研究員和應(yīng)浩研究員,以及上海交通大學王慧教授的大力支持。同時,本研究得到了國家自然科學基金委,科技部重大研發(fā)計劃的資助以及上海營養(yǎng)與健康研究所公共技術(shù)平臺的支持。