2019年9月25日,國(guó)際學(xué)術(shù)期刊Nature Communications在線(xiàn)發(fā)表了肖意傳研究組與秦駿研究組合作的最新研究成果“Modulation of M2 macrophage polarization by the crosstalk between Stat6 and Trim24”。該研究揭示了Stat6乙酰化調(diào)節(jié)巨噬細(xì)胞M2極化,進(jìn)而影響體內(nèi)抗腫瘤免疫的作用機(jī)理,為抗腫瘤免疫的調(diào)控提供了新的分子靶標(biāo)。
腫瘤微環(huán)境中的免疫細(xì)胞構(gòu)成了腫瘤中的免疫調(diào)節(jié)系統(tǒng),其中具有M2型特征的TAMs(tumor associated macrophages, TAMs)在抑制抗腫瘤免疫并促進(jìn)腫瘤進(jìn)程中起到了重要的調(diào)控作用,然而TAMs向M2極化精細(xì)調(diào)控的分子機(jī)制仍不清楚。本研究發(fā)現(xiàn)在巨噬細(xì)胞M2型極化過(guò)程中,調(diào)控極化的關(guān)鍵轉(zhuǎn)錄因子Stat6可以發(fā)生CBP介導(dǎo)的K383位點(diǎn)乙酰化修飾,該位點(diǎn)的乙酰化修飾能夠明顯抑制Stat6的轉(zhuǎn)錄活性以及下游M2型特征基因的表達(dá)。隨后,通過(guò)高通量轉(zhuǎn)錄組測(cè)序(RNA-seq)結(jié)合蛋白質(zhì)譜分析,研究人員發(fā)現(xiàn)了一種Trim家族蛋白的E3泛素連接酶Trim24能夠與乙酰基轉(zhuǎn)移酶CBP結(jié)合,介導(dǎo)CBP蛋白K119位點(diǎn)K63連接的泛素化修飾,增強(qiáng)CBP對(duì)Stat6的招募并促進(jìn)CBP介導(dǎo)的Stat6蛋白K383位點(diǎn)乙酰化修飾,從而抑制Stat6的轉(zhuǎn)錄活性以及巨噬細(xì)胞的M2型極化。
進(jìn)一步的體內(nèi)研究表明,Trim24基因在巨噬細(xì)胞中缺失后抑制了腫瘤微環(huán)境TAMs中Stat6蛋白K383位點(diǎn)的乙酰化修飾,進(jìn)而促進(jìn)了TAMs向M2方向的極化,由此促進(jìn)了腫瘤的生長(zhǎng)。研究人員還發(fā)現(xiàn),乳腺癌病人腫瘤組織中TAMs相較癌旁正常組織中巨噬細(xì)胞表達(dá)更低水平TRIM24與更高水平的M2基因,且腫瘤細(xì)胞條件性培養(yǎng)基能明顯抑制人單核或巨噬細(xì)胞中TRIM24表達(dá)。這些結(jié)果提示腫瘤微環(huán)境可能通過(guò)抑制TAMs中Trim24的表達(dá)進(jìn)而抑制Stat6的乙酰化,從而進(jìn)一步促進(jìn)了TAMs向M2方向極化,并維持了腫瘤中免疫抑制性的微環(huán)境狀態(tài)。因此,靶向Stat6乙酰化修飾或者Trim24活性可以作為腫瘤免疫干預(yù)的潛在分子靶標(biāo)。
 ?
?
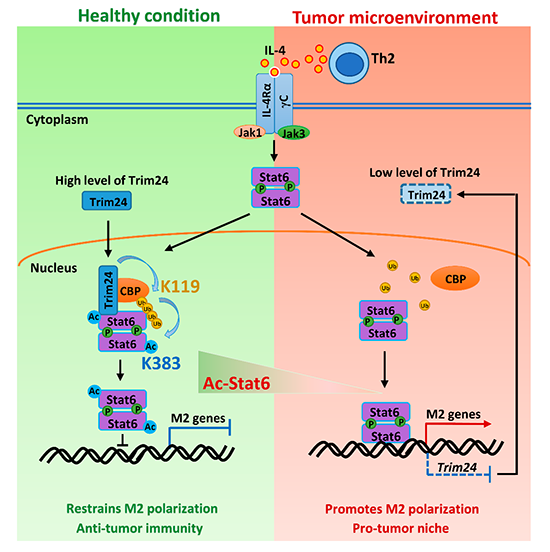
Stat6乙酰化調(diào)節(jié)抗腫瘤免疫的分子機(jī)制
中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所博士后于濤和博士生甘叔誠(chéng)、朱清晨為論文共同第一作者,中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所肖意傳研究員和秦駿研究員為共同通訊作者。該研究得到了江蘇大學(xué)附屬醫(yī)院毛朝明教授、上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院沈坤煒教授等的大力幫助。該研究還得到了科技部、國(guó)家自然科學(xué)基金委及中國(guó)科學(xué)院等項(xiàng)目的資助,同時(shí)也得到了中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所公共技術(shù)平臺(tái)和動(dòng)物平臺(tái)的支持。