2020年7月2日,國際學術期刊Cancer Cell在線發表了中國科學院上海營養與健康研究所秦駿研究組與陸軍軍醫大學大坪醫院江軍主任、南京醫科大學王曉明教授的合作研究論文“SETD2 Restricts Prostate Cancer Metastasis by Integrating EZH2 and AMPK Signaling Pathways”。該研究揭示H3K36甲基轉移酶SETD2響應外界能量信號調控EZH2表達水平,從而抑制前列腺癌轉移的分子機制。
前列腺癌是男性發病率最高的腫瘤,其中轉移性前列腺癌病人的預后極差,因此尋找促進前列腺癌轉移的分子機制具有重要的臨床意義。組蛋白甲基轉移酶SETD2作為哺乳動物中主要的H3K36三甲基轉移酶,被發現在腎癌、膠質瘤、結直腸癌、前列腺癌等多種腫瘤中存在突變,但SETD2的病理功能卻很不明確。此外,SETD2介導的H3K36me3水平與EZH2催化的H3K27me3水平在細胞內呈現互斥現象。但在腫瘤細胞內H3K36me3及H3K27me3的互斥修飾如何實現有待進一步探究。SETD2與EZH2之間是否存在主動調控,其潛在的病理學意義更有待進一步闡明。
研究人員利用小鼠模型及病人數據分析,揭示SETD2的缺失顯著促進前列腺癌的遠端轉移。闡明SETD2通過對EZH2 K735位點甲基化修飾促進EZH2降解,防止細胞轉化為高H3K27me3染色質狀態,進而抑制轉移性前列腺癌的形成的分子機制。EZH2缺失或K735R點突變小鼠模型表明SETD2缺失促進前列腺癌進展主要依賴于其對于EZH2甲基化修飾的調控。有趣的是,SETD2在腫瘤中存在R1523H熱點突變位點。該位點突變后可以抑制SETD2與EZH2相互作用進而缺失EZH2的K735位點甲基化修飾。因此,該突變以不改變H3K36me3修飾的方式促進腫瘤進展。此外,本研究還發現AMPK-FOXO3信號通路可以感受胞外能量變化調控SETD2的表達水平。二甲雙胍激活AMPK-FOXO3-SETD2信號軸可以抑制EZH2高表達前列腺癌的進展。
綜上所述,該研究揭示了SETD2可以響應細胞外能量變化,通過非組蛋白甲基化修飾影響EZH2表達,調節腫瘤細胞內組蛋白修飾狀態,進而影響了前列腺癌的轉移。
中國科學院上海營養與健康研究所博士生袁懷瑞、韓穎和汪學閣為該論文的共同第一作者,秦駿研究員、陸軍軍醫大學大坪醫院江軍主任醫師、南京醫科大學王曉明教授為論文的共同通訊作者。這項工作得到了中科院藥物所譚敏佳研究員、上海交通大學張健教授,李力教授的大力幫助。該研究還得到了科技部、國家自然科學基金委及中國科學院等項目的資助,同時也得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。(科技處)
原文鏈接:https://doi.org/10.1016/j.ccell.2020.05.022
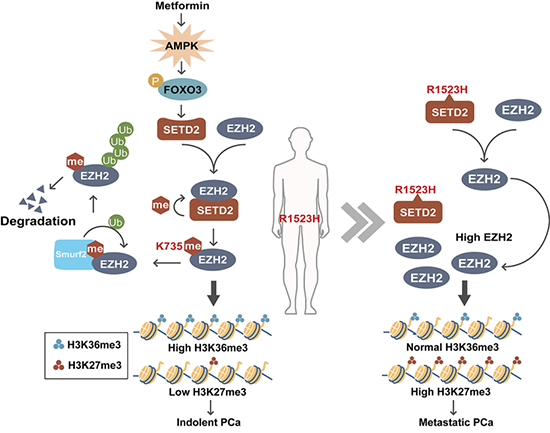
SETD2調控前列腺癌轉移的分子機制示意圖