2020年7月6日,國際學術期刊Nature Cancer在線發表了中國科學院上海營養與健康研究所尹慧勇研究組題為“Aldolase B Suppresses Hepatocellular Carcinogenesis by Inhibiting G6PD and Pentose Phosphate Pathways”的最新研究成果,首次闡明了果糖-1,6-二磷酸(Fructose-1,6-bis-phosphate,FBP)醛縮酶B(Aldolase B, Aldob)在調控肝癌代謝重編程(Metabolic reprogramming)中的作用、機理及臨床意義。
代謝異常是腫瘤的重要特征之一,腫瘤細胞會經歷一系列代謝重編程來滿足自身快速增殖的需要。上世紀20年代提出的瓦博格效應(Warburg Effect)指出:即使在有氧情況下,腫瘤細胞也會以無氧糖酵解來產生能量和細胞增殖所需的原料。因此,腫瘤細胞代謝重編程的分子機制及其臨床意義一直是腫瘤研究領域的重要方向之一。近年的研究發現,腫瘤細胞會利用基因突變、表觀遺傳改變、蛋白相互作用以及代謝酶與代謝物的相互作用等多種機制來實現腫瘤細胞的代謝重編程。Aldolase在糖酵解中催化FBP裂解生成二羥丙酮磷酸(Dihydroxyacetone Phosphate, DHAP)和3-磷酸甘油醛(Glyeraldehyde-3-phosphate, GAP),以及糖異生中由DHAP與GAP生成FBP的逆反應。Aldob主要在肝臟、小腸及腎臟中表達。既往的研究發現Aldob在肝癌組織中表達下調并且其表達與預后相關。但該現象似乎與肝腫瘤細胞的代謝上調矛盾,因此Aldob在肝細胞癌(Hepatocellular Carcinoma, HCC)代謝調控中的分子機制及臨床意義尚待明確。肝癌的發病率在世界范圍內位列所有癌癥的第六位,死亡率更是高居第四位。中國是肝癌大國,每年新增的肝癌病例的55%以上在中國。
本研究中,研究人員從HCC病人組織基因芯片分析入手,發現Aldob在HCC病人腫瘤組織中表達顯著下調,磷酸戊糖途徑的限速酶葡萄糖-6-磷酸脫氫酶(Glucose-6-phosphate dehydrogenase, G6PD)表達顯著上調;Aldob低表達、G6PD高表達的病人生存期短并且預后差,Aldob可作為HCC的獨立風險因素。接著,研究人員利用Aldob全身或者肝臟特異敲除小鼠,在N-亞硝基二乙胺(N-nitrosodiethylamine, DEN)誘導的HCC小鼠模型中發現Aldob敲除后成瘤明顯加重,與癌旁組織相比腫瘤組織G6PD酶活以及PPP代謝流上調;在肝臟特異性敲除Aldob的小鼠中回補Aldob表達顯著抑制腫瘤形成;化學抑制G6PD的酶活或在基因水平下調G6PD的表達均抑制了Aldob缺失誘導的腫瘤形成。機制研究發現,在正常肝細胞中,Aldob與G6PD通過直接的蛋白相互作用來抑制G6PD的酶活;同時,Aldob可以顯著增強抑癌基因p53對G6PD的抑制作用。在腫瘤細胞中,Aldob表達下調解除了對G6PD抑制作用,從而導致PPP代謝增強,提供腫瘤細胞快速生長需要的合成原料以及NADPH 和谷胱甘肽等(如圖所示)。該結果得到了代謝組學以及多種穩定同位素代謝流數據的支持。
綜上,本研究闡明了一種細胞代謝調控的全新分子機制:糖酵解和磷酸戊糖途徑上兩個重要的代謝酶Aldob和G6PD之間的相互作用調控細胞代謝;腫瘤細胞中Aldob的丟失促使其發生代謝重構以促進腫瘤的生長。該研究發現了Aldob一種全新的非酶功能,也提示了Aldob和G6PD的表達及相互作用在肝癌臨床診療中的價值。
中國科學院上海營養與健康研究所尹慧勇研究員、陶用珍助理研究員與海軍軍醫大學第三附屬醫院程樹群主任為該論文通訊作者,中國科學院上海營養與健康研究所博士研究生李敏、何栩曉與海軍軍醫大學第三附屬醫院郭衛星醫生為該論文共同第一作者。該項工作得到了中國科學院分子細胞科學卓越創新中心李黨生研究員、丁建平研究員,中國科學院上海營養與健康研究所李于研究員、以及廈門大學林圣彩和林樹海教授的大力支持。此課題研究得到了國家自然科學基金委、科技部和中國科學院的資助。(科技處)
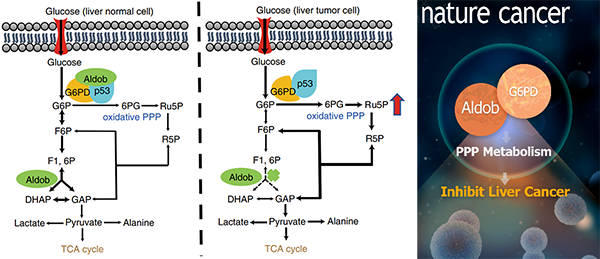
圖. 糖酵解代謝酶Aldob調控肝癌代謝重構的分子機制