2020年10月5日,國際學術期刊PLOS Biology在線發表了中國科學院上海營養與健康研究所中科院腫瘤與微環境重點實驗室肖意傳研究組的研究論文“Peli1 impairs microglial Aβ phagocytosis through promoting C/EBPβ degradation”。該研究揭示了E3泛素連接酶Peli1通過直接介導C/EBPβ泛素化修飾并誘導其降解,進而影響小膠質細胞對β淀粉樣蛋白(Amyloid-β, Aβ)吞噬功能的新機制,該研究為阿爾茲海默病(Alzheimer's Disease, AD)的病理機制與臨床治療提供了新的分子靶標。
AD是一種常見的神經退行性疾病,其特征性病理改變之一為Aβ在腦部大量沉積,從而造成神經元死亡以及認知損傷。在中樞神經系統(Central Nervous System, CNS)內,Aβ的清除主要依賴于小膠質細胞對其的吞噬作用。然而影響并調節小膠質細胞吞噬功能的分子調控機制并不十分明確。
在先前的研究中,肖意傳研究組的科研人員發現Peli1在小膠質細胞中特異性高表達,并介導調節自身免疫性神經炎癥、帕金森氏病(Parkinson's Disease, PD)和病毒性腦炎的發生發展。本研究進一步明確了Peli1在另一種常見神經退行性疾病AD中通過負調控小膠質細胞對Aβ的吞噬能力,致使腦部大量Aβ沉積無法被清除,從而造成AD病情惡化的病理機制。機制研究表明,Peli1直接結合并介導轉錄因子C/EBPβ的泛素化及降解,由于C/EBPβ是清道夫受體CD36的關鍵轉錄因子,故Peli1敲除后顯著促進了CD36基因的表達,由此增強了小膠質細胞對Aβ的吞噬作用。因此,在老年Peli1基因缺失的5×FAD轉基因AD模型小鼠腦內,小膠質細胞對Aβ的清除作用顯著增強,由此抑制了Aβ在腦部的沉積。此外,在5×FAD小鼠腦部小膠質細胞和AD病人腦組織中,Peli1的表達較正常對照明顯升高,提示AD病理會誘導小膠質細胞中Peli1的表達。因此,小膠質細胞中Peli1是AD診治的一個潛在新分子靶標。
中國科學院上海營養與健康研究所助理研究員許靜和博士后于濤為論文共同第一作者。中國科學院上海營養與健康研究所肖意傳研究員、江蘇大學附屬醫院毛朝明為該論文共同通訊作者。該工作得到了意大利維羅納大學Gabriela Constantin教授等的大力支持。該研究還得到了中國科學院、科技部、國家自然科學基金委及江蘇省科學技術廳等項目的資助,同時也得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
原文鏈接:https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3000837
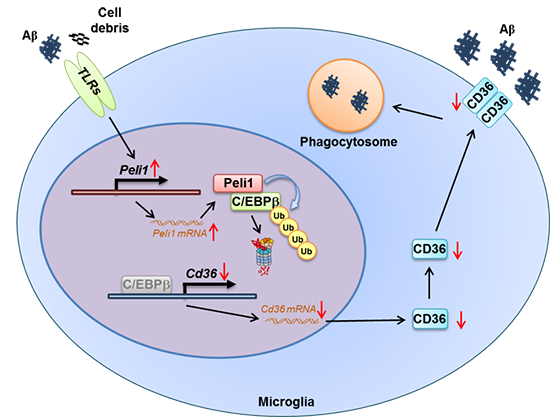
Peli1調節小膠質細胞介導的Aβ吞噬與AD病理模式圖