2020年11月25日,國際學術期刊Science Advances在線發表了中國科學院上海營養與健康研究所王瑩、時玉舫研究組題為“IGF2R-initiated proton rechanneling dictates an anti-inflammatory property in macrophages”的研究成果,闡明了胰島素樣生長因子2(insulin like growth factor 2, IGF2)分別通過激活胰島素樣生長因子2受體(insulin like growth factor 2 receptor, IGF2R)和胰島素樣生長因子1受體(insulin like growth factor 1 receptor, IGF1R)賦予巨噬細胞抗炎和促炎潛能的新機制,揭示了胰島素樣生長因子家族成員調控天然免疫記憶的核心規律。
該研究組于2019年在Cell Metabolism上報道了他們干細胞研究的新發現。低氧處理的間充質干細胞借以IGF2,預編程巨噬細胞的氧化磷酸化代謝傾向性并決定其抗炎特性,有效地抑制自身免疫性疾病。在此基礎上,王雪楓博士等發現IGF2對于自身免疫性疾病的治療作用和對巨噬細胞的調控與劑量密切相關——低劑量IGF2促進抗炎巨噬細胞的形成從而緩解疾病,然而高劑量IGF2有利于促炎巨噬細胞的形成而加重疾病。鑒于IGF2與IGF2R的親和力高于其與IGF1R的親和力,IGF2雙向調節自身免疫性疾病的特性可能與其差異性激活IGF1R和IGF2R有關,為此,研究構建了髓系細胞條件性敲除IGF1R或IGF2R的小鼠,并證明IGF2對于抗炎巨噬細胞的調控依賴于IGF2R,而其對促炎巨噬細胞的調節則主要依賴于IGF1R。通過一系列機制研究,證明低劑量IGF2優先結合IGF2R,誘導IGF2R向細胞核內化,核內IGF2R促進GSK3α/β與染色質結合來激活Dnmt3a表達,維持V型ATP酶相關基因的高甲基化狀態,從而抑制V型ATP酶表達,導致溶酶體酸化受限,積累在細胞質中的H+以順化學梯度方式進入線粒體膜間隙,推動氧化磷酸化,賦予巨噬細胞抗炎記憶。研究人員將這個H+向溶酶體內化受限,轉而進入線粒體膜間隙的過程命名為質子改道(proton rechanneling)。此外,研究證明,高劑量IGF2不但結合IGF2R,還可以快速激活IGF1R-AKT信號通路,通過磷酸化GSK3α/β并抑制其功能,阻斷質子改道,促進有氧糖酵解,使得巨噬細胞具有促炎功能。此外,研究發現靶向性激活IGF2R,賦予巨噬細胞抗炎記憶,顯著抑制腹膜炎和炎癥性腸病。研究表明天然免疫具有強大的免疫調控能力,維持正常機體的免疫穩態,在代謝性疾病、癌癥、感染等發揮重要作用。天然免疫調控的持續性以及是否有適應性免疫的相似的記憶,一直是科學家關注的熱點。本項研究發現IGF2R靶向活化引起質子在溶酶體和線粒體中的重分布機制及其在決定巨噬細胞抗炎特性中的關鍵作用,為理解天然免疫和自身免疫性疾病和炎癥性疾病治療調控了新的靶標和治療策略。
中國科學院上海營養與健康研究所王瑩研究員、時玉舫研究員為共同通訊作者,博士畢業生王雪楓為第一作者,研究還得到了美國Rutgers大學Arthur I. Roberts博士、蘇州大學邵常順教授和意大利羅馬第二大學Gerry Melino教授的合作支持。本項研究得到了科技部國家重點研發計劃、中國科學院戰略性先導專項、國家自然科學基金委、中國-意大利衛生部合作基金、中國博士后科學基金、中國科學院上海營養與健康研究所腫瘤微環境重點實驗室開放課題等項目的資助。同時,感謝上海營養與健康研究所公共技術平臺以及動物平臺的支持。
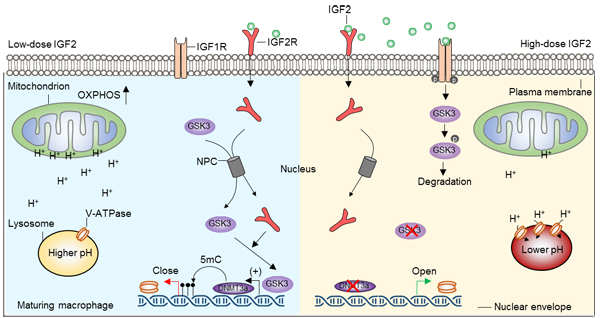
圖:IGF2分別通過激活IGF2R和IGF1R決定巨噬細胞抗炎潛能和促炎潛能