2021年4月29日,國際學術期刊Journal of Experimental Medicine在線發表了中國科學院上海營養與健康研究所肖意傳研究組等的合作研究論文“BFAR coordinates TGFβ signaling to modulate Th9-mediated cancer immunotherapy”。該研究發現腫瘤來源的TGFβ能夠負調控CD4+ T細胞中BFAR基因的表達,進而抑制TH9分化及其介導的腫瘤免疫治療效果,并揭示下游具體的分子調控機制。
腫瘤免疫治療作為一種新興的腫瘤治療手段,已成為目前全球腫瘤臨床治療與研究中最具前景的方向之一,特別在面臨患者腫瘤復發、化療藥物耐受、腫瘤無法手術切除等臨床問題時能提供新的有效策略。近年來,PD-1/PD-L1阻斷療法已被運用于多種腫瘤的治療中,可通過增強機體的抗腫瘤免疫反應來發揮功能。然而,這種療法只對一小部分病人有效,因此研究機體對該療法不敏感的機制是改善免疫檢查點治療腫瘤的效果和開發相關新藥物的關鍵。TGFβ作為一種免疫抑制因子,已被報道在多種腫瘤組織中表現為高表達,并能介導腫瘤免疫逃逸的發生,阻斷TGFβ可大大增強免疫檢查點療法的治療效果。然而,腫瘤患者體內高水平的TGFβ介導免疫逃逸發生的具體機制仍不清楚。
TH9細胞是一類具有顯著抗實體腫瘤作用的CD4+ T細胞亞群,其不僅可以高效的殺傷并清除實體腫瘤,而且還能有效的抑制腫瘤的轉移和復發。眾所周知,TGFβ能夠參與誘導TH9細胞的產生,那么,TGFβ是否也能通過促進體內TH9細胞的產生而發揮抗腫瘤的作用?與預期相反的是,該研究發現,結直腸癌和胃癌病人外周血中的TGFβ水平與TH9特征性細胞因子IL-9的濃度呈負相關性,其原因是腫瘤病人血漿中相對較高濃度的TGFβ會抑制CD4+ T細胞中BFAR基因的表達,并通過這種負反饋調節作用抑制TGFβ信號通路的活化和CD4+ T細胞向TH9細胞的分化,進而減弱機體的抗腫瘤免疫反應。進一步的機制研究發現,BFAR能夠介導TGFβR1第268位賴氨酸發生K63連接的泛素化,而這一過程對于維持TGFβ信號通路的活性至關重要。因此BFAR基因的缺失或者TGFβR1第268位賴氨酸位點的突變會導致TGFβR1的泛素化修飾受到抑制,進而阻止TGFβ信號通路的激活和TH9細胞的分化。該研究隨后利用不同的腫瘤模型對BFAR的抗腫瘤功能進行驗證后發現,在小鼠皮下黑色素瘤模型和肺轉移模型中,BFAR過表達的TH9細胞具有顯著的抗腫瘤功效并可以增加PD-1抗體介導的免疫檢查點治療的敏感性。除此之外,該研究還使用了結直腸癌病人來源的腫瘤異種移植(PDX)模型,發現靶向BFAR基因進行改造的腫瘤病人來源的TH9細胞同樣具有非常好的抗腫瘤效果。
綜上所述,該研究證明,BFAR作為TGFβ調控的關鍵靶點,能夠通過反饋作用精細調控TGFβ信號通路的激活和TH9細胞的分化,從而為增強TH9介導的腫瘤免疫療法的治療效果提供了新的策略。
中國科學院上海營養與健康研究所博士生裴思雨為該論文的第一作者,肖意傳研究員、江蘇省腫瘤醫院戴東方副主任醫師、上海市胸科醫院羅清泉主任醫師、浙江大學附屬邵逸夫醫院溫珍珍研究員為論文的共同通訊作者。這項工作得到了浙江大學張龍教授,江蘇大學于峰教授以及西湖大學常興教授的大力支持與幫助。此外,本研究還獲得了國家重點研發計劃、國家自然科學基金項目、中國科學院戰略性先導科技專項、浙江省醫學衛生科學基金項目以及中國科學院腫瘤與微環境重點實驗室的資助,同時也得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
原文鏈接:https://doi.org/10.1084/jem.20202144
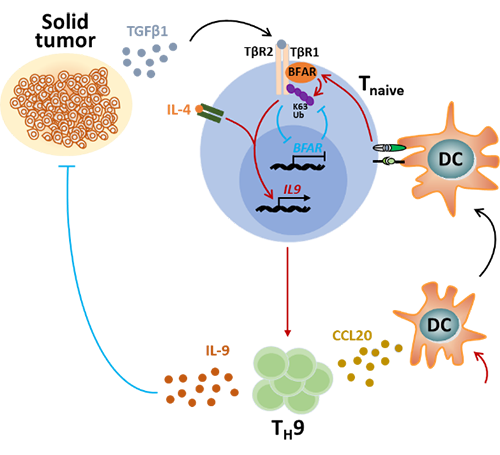
BFAR靶向TGFβ信號通路調控TH9的分化及其介導的抗腫瘤免疫反應機制示意圖