2021年9月2日,國(guó)際學(xué)術(shù)期刊Nature Communications在線發(fā)表了中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所胡國(guó)宏研究組題為”Long non-coding RNA NR2F1-AS1 induces breast cancer lung metastatic dormancy by regulating NR2F1 and ΔNp63”的最新研究成果,闡釋了長(zhǎng)鏈非編碼RNA NR2F1-AS1在乳腺癌細(xì)胞肺轉(zhuǎn)移休眠調(diào)控中的功能、作用機(jī)制及臨床意義。
乳腺癌是女性健康的主要威脅之一,乳腺癌細(xì)胞轉(zhuǎn)移到肺、腦、肝、骨等重要器官是乳腺癌患者死亡的主要原因。在轉(zhuǎn)移過程中,播散到遠(yuǎn)端器官的腫瘤細(xì)胞往往會(huì)進(jìn)入休眠狀態(tài),其特點(diǎn)是增殖緩慢、持續(xù)存活、對(duì)輔助化療等治療策略耐受。轉(zhuǎn)移休眠在臨床上是一種威脅,因?yàn)閱蝹€(gè)腫瘤細(xì)胞或微小轉(zhuǎn)移病灶可以存在數(shù)月、數(shù)年甚至數(shù)十年而無法被發(fā)現(xiàn),且有可能重新激活并導(dǎo)致腫瘤復(fù)發(fā)。長(zhǎng)期以來,人們已經(jīng)認(rèn)識(shí)到腫瘤細(xì)胞轉(zhuǎn)移休眠的臨床重要性。然而,我們對(duì)于轉(zhuǎn)移休眠的調(diào)節(jié)機(jī)制認(rèn)識(shí)還存在諸多空白。
先前的研究已經(jīng)注意到,休眠的腫瘤細(xì)胞可能具有正常干細(xì)胞的生長(zhǎng)停滯和多能性特征。更重要的是,休眠的腫瘤細(xì)胞在長(zhǎng)期靜止后保留了引發(fā)新腫瘤的能力,這是腫瘤干細(xì)胞樣細(xì)胞(Cancer Stem-like Cells, CSCs)的一個(gè)決定性特征。但是,目前對(duì)腫瘤細(xì)胞干性特征與轉(zhuǎn)移休眠關(guān)系的研究結(jié)論并不一致。CSCs是指具有增強(qiáng)腫瘤啟動(dòng)能力的腫瘤細(xì)胞亞群,事實(shí)上,它們本身可能是異質(zhì)的。目前的研究表明,在乳腺癌中存在以CD24-CD44+為標(biāo)志物具有間質(zhì)樣特征的CSC(M-BCSC)和以ALDH+為標(biāo)志物具有上皮樣特征的CSC(E-BCSC)兩個(gè)不同群體。有趣的是,功能研究表明E-BCSC比M-BCSC具有更強(qiáng)的增殖能力和成瘤性,而M-BCSCs往往是靜止的。這與上皮間質(zhì)轉(zhuǎn)化(Epithelial-Mesenchymal Transition, EMT)后腫瘤細(xì)胞趨于生長(zhǎng)受阻的觀點(diǎn)一致。這些研究表明CSCs的異質(zhì)性可能為關(guān)于CSCs在轉(zhuǎn)移休眠中作用的不一致提供解釋。
此項(xiàng)研究發(fā)現(xiàn),M-BCSC相較E-BCSC具有更強(qiáng)的從原位瘤向外播散的能力,但是播散到肺部的E-BCSC更容易快速形成轉(zhuǎn)移灶而M-BCSC則傾向于在肺部休眠。通過轉(zhuǎn)錄組測(cè)序分析發(fā)現(xiàn),長(zhǎng)鏈非編碼RNA NR2F1-AS1在休眠的M-BCSC中上調(diào)。功能研究表明NR2F1-AS1能夠通過促進(jìn)腫瘤細(xì)胞的EMT提升乳腺腫瘤細(xì)胞的M-BCSC特征從而促進(jìn)原位腫瘤細(xì)胞向外播散,同時(shí)NR2F1-AS1能夠抑制播散到肺部腫瘤細(xì)胞的E-BCSC特征從而抑制腫瘤細(xì)胞在肺部的再激活,最終促進(jìn)乳腺癌細(xì)胞的轉(zhuǎn)移休眠。病人來源的腫瘤樣本分析也證實(shí)NR2F1-AS1與腫瘤細(xì)胞干性特征和轉(zhuǎn)移休眠存在明顯的相關(guān)性。
綜上所述,這一研究闡釋了NR2F1-AS1在乳腺癌細(xì)胞肺轉(zhuǎn)移休眠調(diào)控中的功能機(jī)制,并從BCSCs異質(zhì)性角度解釋了CSCs在轉(zhuǎn)移休眠中的作用,對(duì)于我們理解腫瘤細(xì)胞的轉(zhuǎn)移休眠具有重要理論意義。
中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所胡國(guó)宏研究員為該論文通訊作者,博士研究生劉英杰和博士后張沛淵為共同第一作者。該工作還得到了華東師范大學(xué)生命科學(xué)學(xué)院上海市調(diào)控生物學(xué)重點(diǎn)實(shí)驗(yàn)室廖魯劍教授、山東大學(xué)附屬齊魯醫(yī)院楊其峰、上海交通大學(xué)附屬第六人民醫(yī)院楊慶誠(chéng)教授和復(fù)旦大學(xué)附屬華山醫(yī)院欽倫秀教授的合作支持。此課題研究得到了中國(guó)科學(xué)院、中國(guó)科學(xué)技術(shù)部、國(guó)家自然科學(xué)基金委和中國(guó)博士后科學(xué)基金的資助。
文章鏈接:https://www.nature.com/articles/s41467-021-25552-0
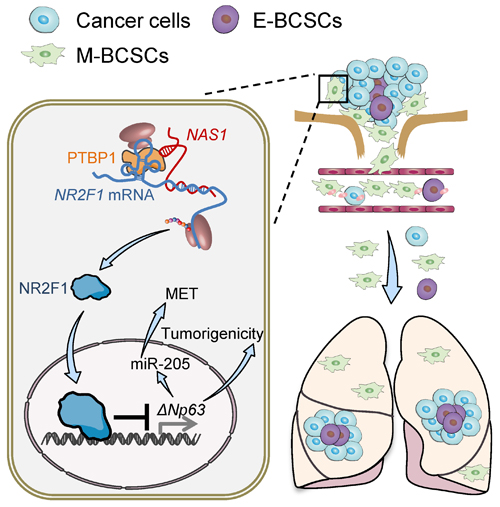
圖. NR2F1-AS1通過NR2F1-ΔNp63信號(hào)通路調(diào)控乳腺癌細(xì)胞轉(zhuǎn)移休眠的分子機(jī)制模式圖