2022年2月16日,國際學術期刊Nature Communications在線發表了中國科學院上海營養與健康研究所詹麗杏研究組題為“Lin28B-high breast cancer cells promote immune suppression in the lung pre-metastatic niche via exosomes and support cancer progression”的最新研究成果,闡釋了多潛能因子Lin28B在乳腺癌轉移前肺組織免疫微環境調控中的作用、機制和臨床意義。
三陰性乳腺癌是惡性程度最高的乳腺癌亞型,臨床上以侵襲性強、易復發和轉移為主要表現。由于雌激素受體、孕激素受體和HER2 擴增的缺乏,使得其對內分泌治療和靶向治療均不敏感,目前主要依靠化療和放療,約40~50%患者在接受根治手術后仍出現復發和轉移,患者平均5年生存率不足15%。因此研究乳腺癌尤其是三陰性乳腺癌早期轉移機制,揭示干預新靶點是當前亟待解決的問題。
在腫瘤生長早期階段,肺組織即可有腫瘤細胞到達,到達的腫瘤細胞有的處于生長停滯的靜止狀態,有的則啟動轉移灶的形成,那么發生轉移的肺組織免疫微環境有什么規律呢?研究表明,腫瘤細胞的局部生長受到周圍環境的調節,如肺基質細胞分泌的因子由于抑制腫瘤生長而使細胞處于休眠狀態。那么,這些轉移細胞的免疫監控是如何被抑制從而啟動轉移,并且原位腫瘤遠程調控肺組織微環境及其免疫細胞活性狀態的機制是什么,我們仍所知甚少。
在本研究中,研究人員首先依據人乳腺癌組織芯片樣本和公共數據庫信息,發現多潛能因子Lin28B的高表達與乳腺癌(特別是三陰性乳腺癌)患者預后不良密切相關,Lin28B高表達特異促進肺轉移,與骨轉移和腦轉移無關。進一步,研究人員通過特定乳腺癌原位移植小鼠模型證明了Lin28B的促轉移前免疫微環境抑制作用,而這是乳腺癌肺轉移關鍵因素。機制上,他們發現,Lin28B表達使轉移前肺組織中性粒細胞聚集增多和N2轉化新機制,證實PD-L2和異常表達的細胞因子流調控N2轉化的中性粒細胞增高,從而抑制轉移前肺組織CD4+/CD8+ T細胞的增殖、活化和Th1分化,因而促進局部抑制性免疫微環境形成。在此基礎上,他們發現原發腫瘤外泌體足以誘導轉移前肺組織免疫抑制和肺轉移發生,Lin28B表達使原位腫瘤內ALDH+干細胞比例上調,這群細胞分泌的外泌體由包含低含量的let-7s家族成員,導致轉移前肺組織成纖維細胞、中性粒細胞和巨噬細胞分別釋放增多的CXCLs、IL-6和IL-10,由此引起中性粒細胞召集和N2轉化。因此,當采用IL-6和PD-L2的聯合干預,明顯解除轉移前肺組織的免疫抑制,抑制Lin28B引起的肺轉移,表明免疫抑制是Lin28B引起肺轉移的關鍵機制以及早期機制。
綜上,該研究發現Lin28B經外泌體途徑,調節轉移前肺組織細胞因子表達進而改變中性粒細胞表型和T細胞免疫狀態產生肺轉移的作用機理。由于Lin28B在三陰性乳腺癌中的廣泛表達,本研究也提示,免疫抑制可能是三陰性乳腺癌肺轉移早期微環境普遍存在的機制,這一線索為免疫治療方法干預肺早期微環境提供了新思路。
中國科學院上海營養與健康研究所詹麗杏研究員為該論文通訊作者,祁美艷副研究員和華中科技大學附屬同濟醫院甲乳外科夏耘副主任醫師為共同第一作者。該研究獲得了國家重點研發計劃項目、國家自然科學基金委項目、恩施州科技計劃研究與開發等項目的資助。
文章鏈接:https://www.nature.com/articles/s41467-022-28438-x
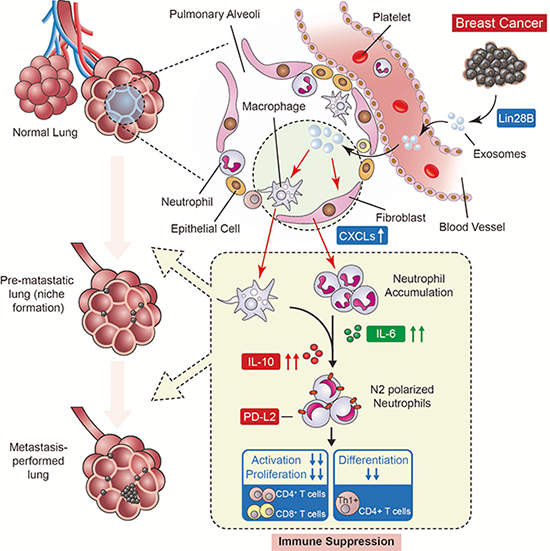
圖注:Lin28B通過外泌體調節轉移前肺組織免疫抑制促進乳腺癌轉移新機制