2022年11月10日,中國科學院上海營養與健康研究所應浩研究團隊在學術期刊Journal of Molecular Cell Biology正式發表了題為“Aberrant elevation of FTO levels promotes liver steatosis by decreasing the m6A methylation and increasing the stability of SREBF1 and ChREBP mRNAs”的研究論文。該研究發現了脂肪量和肥胖相關(fat mass and obesity-associated,FTO)基因在胰島素調節的肝臟脂肪生成和NAFLD發病過程中的關鍵機制。肝臟FTO能去甲基化并穩定SREBF1和ChREBP的mRNA,從而上調負責肝臟脂肪生成的關鍵脂肪生成酶的表達水平,導致出現肝臟脂肪變性。此外,胰島素可誘導肝臟FTO的表達,FTO介導胰島素的部分脂肪生成作用。最后,抑制FTO可以減少肝臟脂肪生成和TG積累,暗示FTO可以作為治療NAFLD的潛在靶點。
NAFLD已成為最常見的慢性肝病,發病率高于T2DM和肥胖癥。它也是全球肝臟相關死亡率中增長最快的因素,目前還沒有FDA批準的藥物。NAFLD的標志是肝TG積累。一系列研究表明,增加TG產生(脂肪酸攝取和DNL)而不是減少動員(脂肪酸氧化和VLDL輸出)是NAFLD發展的主要機制,其中DNL可能是NAFLD發病的重要驅動因素。許多DNL酶,如ACLY、ACC1、FASN和SCD1,受關鍵轉錄因子(SREBP1c和ChREBP)的協調調節。
N6-甲基腺苷(m6A)是最豐富的表觀遺傳修飾,至少分布在四分之一的哺乳動物mRNA中,在各種生理病理過程中調控mRNA代謝。m6A修飾是由一組名為甲基轉移酶(Writer)和去甲基酶(Eraser)的酶動態控制的。m6A修飾可以被甲基閱讀蛋白(Reader)識別。FTO是通過全基因組關聯研究(GWAS)鑒定的肥胖易感基因,有研究發現嚙齒動物和NAFLD患者的脂肪肝中FTO表達水平增加。盡管知道FTO參與調節肝臟脂肪生成,但FTO在肝臟脂肪生成中的生理病理作用尚不完全清楚。
該研究發現,小鼠非酒精性脂肪肝中,總RNA m6A甲基化減少,并伴隨著FTO表達的增加。肝臟過表達FTO在體內和體外均能促進脂肪變性。在肝細胞中,FTO過表達能特異性地上調負責脂肪生成的基因,但不影響參與脂肪酸攝取/氧化或脂蛋白輸出的基因。從機制上講,FTO可以通過m6A去甲基化來穩定SREBF1和ChREBP的mRNA,從而導致其蛋白質水平增加。胰島素治療在體內和體外均可增加FTO表達。抑制FTO的去甲基化酶活性可以降低SREBF1、ChREBP以及脂肪生成基因的表達,從而改善小鼠脂肪肝中TG的積累。該研究發現了“胰島素/FTO/SREBP1c/ChREBP/脂肪生成”信號通路,鞏固了FTO是NAFLD重要貢獻者的結論。FTO通過去甲基酶活性,在肝臟脂肪代謝中增加了一層動態的基因表達調控機制。靶向肝臟FTO作為治療NAFLD的策略,在未來值得進一步探討。
中國科學院上海營養與健康研究所博士研究生唐志立為該論文的第一作者,應浩研究員、博士研究生李卓陽和復旦大學附屬醫院中山醫院蔣晶晶博士為本文的通訊作者。該研究得到了科技部及基金委項目的支持,同時也得到中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
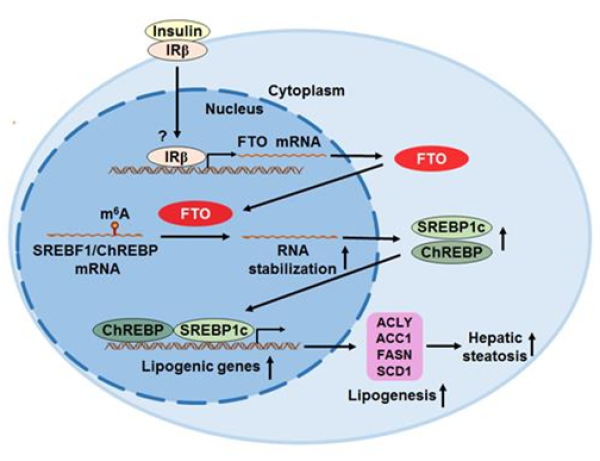
圖注 FTO信號通路示意圖
注:胰島素刺激肝細胞后,FTO的表達增加。FTO可以通過m6A去甲基化來穩定SREBF1和ChREBP的mRNA,從而導致其蛋白質水平增加,最終促進了肝臟脂肪生成,導致肝臟脂肪變性。
原文鏈接:https://doi.org/10.1093/jmcb/mjac061
?