2023年3月18日,中國科學院上海營養與健康研究所丁秋蓉研究組在國際期刊Nature Communications在線發表了題為“Acute liver steatosis translationally controls the epigenetic regulator MIER1 to promote liver regeneration in a study with male mice”的研究論文。該研究發現肝臟再生過程中,肝實質細胞的MIER1表觀因子響應脂質動態改變,從而調控肝實質細胞增殖再生的機制。
哺乳動物的健康肝臟組織在肝損傷后具有強大的再生能力。作為一種“新建再生”,在肝臟組織經歷2/3肝切或者急性毒性損傷后,處于靜息期的肝臟細胞(主要為肝實質細胞)會重新進入細胞周期進行增殖,生成新的肝臟細胞,在不到兩周的時間內恢復全部的肝臟質量和功能。但肝臟再生能力在脂代謝紊亂的肝臟組織中顯著減弱,如酒精或非酒精性脂肪肝、衰老肝臟等,導致肝臟損傷后無法完全恢復細胞數量和正常功能,促進了肝纖維化、肝硬化等終末期肝病的發展。同時,臨床肝臟移植手術中,供體肝臟的脂代謝異常(如脂肪肝)也會導致其無法在受體內正常增殖,導致“小肝癥”和移植手術的失敗。
肝臟脂質代謝穩態對維持肝臟再生潛能非常關鍵,如在肝臟再生早期會出現明顯的急性脂質積累,并且抑制上述急性脂質積累會嚴重影響肝臟再生。但脂質穩態如何調控肝臟再生,同時脂代謝紊亂的肝臟為何再生潛能下降,其背后的分子機制均不清晰。
為了揭示肝臟再生過程中未知的關鍵調控因子,研究人員構建了肝臟再生的體內大規模CRISPR篩選平臺,篩選鑒定出MIER1為關鍵再生調控因子。MIER1為中胚層誘導早期反應蛋白(mesoderm induction early response 1),前期關于其研究較少,尚無MIER1在調控肝臟再生或者肝臟功能中的研究。研究人員通過肝切實驗發現MIER1作為一個表觀調控因子,在肝臟再生過程中起表觀“剎車”的作用:MIER1大量結合在細胞增殖相關基因的轉錄起始區域,抑制細胞增殖基因的表達,敲除MIER1可顯著促進細胞增殖相關基因的開放程度,提高增殖相關基因的表達,促進肝臟再生。
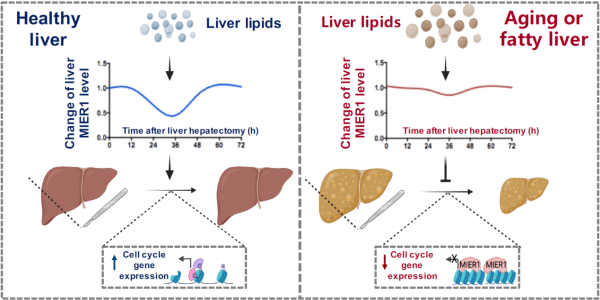
研究人員同時發現在肝切后小鼠的再生過程中,MIER1水平出現了短暫的蛋白表達量下調,并在再生完成后期恢復到肝切前水平,提示肝臟再生過程中存在MIER1的動態調控機制。進一步研究發現,MIER1響應肝臟再生過程中的脂質急性積累,而脂質急性積累通過調控MIER1的蛋白水平行使重要的表觀調控功能(圖1):肝臟脂質急性積累誘發肝實質細胞的急性應激反應,導致核糖體翻譯過程的短暫抑制,從而影響MIER1蛋白翻譯,引起MIER1蛋白水平的動態下調;而MIER1蛋白的下調會進一步促進染色質開放、細胞周期基因表達和肝臟再生。更有意思的是,此生理調控過程在衰老肝臟和高脂誘導的脂肪肝中明顯受損,導致MIER1一直處于一個高表達狀態,從而持續抑制細胞周期基因的表達;而敲除MIER1后衰老肝臟和高脂誘導的脂肪肝再生能力明顯提高。
綜上所述,該研究發現肝臟再生過程中脂質的動態改變調控了肝臟再生事件的進行,通過大規模體內篩選鑒定出表觀因子MIER1是介導脂質動態信號轉變為修復再生信號的關鍵“橋梁”因子。在健康肝臟中,再生早期脂質變化誘導的MIER1動態下調促進了肝臟再生;而在肝臟脂肪代謝紊亂條件下,MIER1的持續表達抑制了肝臟再生。研究體現了正常肝臟再生過程中脂質代謝的時空變化與表觀重塑的高度協同性,以及病理狀態中上述協同性受損對肝臟再生修復的影響,提出了病理狀態下促進肝臟再生的潛在策略。
中國科學院上海營養與健康研究所丁秋蓉研究員為本論文通訊作者,博士生陳彥好(現為博后)、陳蘭蘭和吳曉珊為本論文共同第一作者。陳彥好博士為共同通訊作者。研究得到了中科院上海營養與健康研究所秦駿、應浩和周犇研究員,上海交通大學附屬第六人民醫院胡承教授的大力支持。研究同時得到中國科學院戰略性先導科技專項、國家自然科學基金等項目基金的資助,以及中國科學院上海營養與健康研究所公共技術中心的技術支持。
 ?
?
圖1: 肝臟急性脂肪變性通過MIER1促進肝臟再生功能的機制模式圖