2019年6月10日,《自然》Nature雜志在線發表了題為“Off-target RNA mutation induced by DNA base editing and its elimination by mutagenesis”的研究論文,該研究由中國科學院神經科學研究所、腦科學與智能技術卓越創新中心楊輝研究組、四川大學華西二院/生命科學學院郭帆研究組和中國科學院上海營養與健康研究所隸屬的計算生物學研究所(中國科學院-馬普學會計算生物學研究所)李亦學研究組合作完成,該研究發現DNA單堿基編輯工具CBE和ABE均存在大量的RNA脫靶效應,相比于僅有GFP處理的對照組,CBE或ABE處理的細胞的RNA SNV平均增加了15倍之多。研究者通過一系列分析證明這些RNA脫靶產生的單核苷酸突變與目的編輯位點沒有序列相似性,而主要是由于DNA單堿基編輯器的脫氨酶APOBEC1 (BE3)和TadA (ABE)所導致的。此外,團隊還發現很高比例的RNA脫靶發生在癌基因和抑癌基因上,如果用于臨床治療有較大的致癌風險。結合今年3月在《科學》雜志報道單堿基編輯技術BE3存在全基因組范圍內的DNA脫靶效應,該項研究發現了單堿基編輯工具還存在無法預測的RNA脫靶,加強了世人對單堿基編輯工具的安全性的審視。
為了獲得更加精準的單堿基編輯工具,研究團隊通過引入突變的方法對兩種DNA單堿基編輯器的胞嘧啶脫氨酶和腺嘌呤脫氨酶分別進行了優化,最終獲得了3種高保真度的BE3突變體,均能夠完全消除RNA脫靶并維持DNA編輯活性的高精度單堿基編輯工具。針對ABE系統,根據降低脫氨酶TadA*的RNA結合活性的思路進行點突,在降低RNA脫靶現象的同時維持了其在DNA上的編輯活性。此外,團隊開發的ABE(F148A)突變體還能夠縮小編輯窗口,實現更加精準的DNA編輯。該技術在特異性和精確性上超越了ABE7.10,結合之前的研究ABE并不造成DNA上的脫靶,該突變體有望在未來成為一種更加安全、更加精準的基因編輯工具,應用于臨床治療中。
上述工作是眾多研究組共同合作的重要成果,得到神經所流式分選平臺,巴斯德所流式分選平臺的大力協助。本工作得到國家高科技研發項目,中科院戰略性先導科技專項,國家自然科學基金委員會和上海市科學技術委員會等項目的資助。
原文鏈接:https://www.nature.com/articles/s41586-019-1314-0
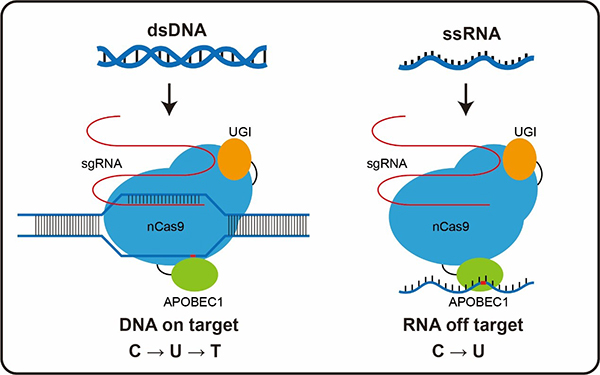
圖注.單堿基編輯器BE3中的脫氨酶除了誘導DNA的胞嘧啶脫氨基轉變成T,還能在RNA上造成大范圍的脫靶。